கோபால்ட்(II) ஆக்சைடு
கோபால்ட்(II) ஆக்சைடு (Cobalt(II) oxide or cobalt monoxide) என்பது CoO என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். சிவப்பு ஆலிவ் பச்சை படிகங்களாக அல்லது சாம்பல் அல்லது கருப்பு தூளாக இச்சேர்மம் தோற்றமளிக்கிறது[3] . பீங்கான் தொழிலில் நீலநிறப் பளிங்கை உருவாக்கும் கூட்டுப்பொருளாகவும் மிளிரியாகவும் வேதித் தொழிற்சாலைகளில் கோபால்ட்(II) உப்புகளைத் தயாரிக்கவும் பயன்படுத்தப்படுகிறது.
 | |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
கோபால்ட்(II) ஆக்சைடு | |
| வேறு பெயர்கள்
கோபால்டசு ஆக்சைடு கோபால்ட் ஓராக்சைடு | |
| இனங்காட்டிகள் | |
| 1307-96-6 | |
| ChemSpider | 8117730 |
| EC number | 215-154-6 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image Image |
| பப்கெம் | 9942118 |
| வே.ந.வி.ப எண் | GG2800000 |
SMILES
| |
| UN number | 3288 |
| பண்புகள் | |
| CoO | |
| வாய்ப்பாட்டு எடை | 74.9326 கி/மோல் |
| தோற்றம் | கருப்புநிறத் தூள் |
| மணம் | நெடியற்றது |
| அடர்த்தி | 6.44 கி/செ.மீ3 [1] |
| உருகுநிலை | |
| தண்ணீரில் கரையாது[2] | |
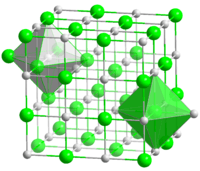
| கட்டமைப்பு | |
| படிக அமைப்பு | கனசதுரம், cF8 |
| புறவெளித் தொகுதி | Fm3m, No. 225 |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | ICSC 1551 |
| ஈயூ வகைப்பாடு | தீங்கானது (Xn) சுற்றுச் சூழலுக்கு அபாயமானது (N) |
| R-சொற்றொடர்கள் | R22, R43, R50/53 |
| S-சொற்றொடர்கள் | (S2), S24, S37, S60, S61 |
| தீப்பற்றும் வெப்பநிலை | எளிதில் தீப்பற்றாது |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose) |
202 மி.கி/கி.கி |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | கோபால்ட்(II) சல்பைடு கோபால்ட்(II) ஐதராக்சைடு |
| ஏனைய நேர் மின்அயனிகள் | இரும்பு(II) ஆக்சைடு நிக்கல்(II) ஆக்சைடு |
| தொடர்புடைய சேர்மங்கள் | கோபால்ட்(II,III) ஆக்சைடு கோபால்ட்(III) ஆக்சைடு |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
அமைப்பு மற்றும் பண்புகள்
அணிக்கோவை மாறிலி மதிப்பு 4.2615 Å உள்ள பெரிகிளாசு (பாறை உப்பு) அமைப்பை கோபால்ட்(II) ஆக்சைடு படிகங்கள் ஏற்றுள்ளன[4].
16°செல்சியசு வெப்பநிலைக்குக் கீழ் எதிரயகாந்தப்பொருளாக உள்ளது[5].
தயாரிப்பு
950° செல்சியசு வெப்பநிலையில் கோபால்ட் (II,III) ஆக்சைடு சிதைவடைந்து கோபால்ட்(II) ஆக்சைடாக மாறுகிறது.:[6]
- 2 Co3O4 → 6 CoO + O2
வர்த்தகரீதியாக கிடைத்தாலும் கோபால்ட்(II) ஆக்சைடு ஆய்வகங்களிலும் கோபால்ட்(II) குளோரைடு கரைசலை மின்னாற்பகுப்பு முறையில் தயாரிக்கிறார்கள்[7]
CoCl2 + H2O → CoO + H2 + Cl2.
கோபால்ட் ஐதராக்சைடை வெப்ப நீர்நீக்கம் செய்து பின்னர் வீழ்படிவாக்கும் முறையிலும் கோபால்ட்(II) ஆக்சைடை தயாரிக்கப்படுகிறது.
- CoX + 2 KOH → Co(OH)2 + K2X
- Co(OH)2 → CoO + H2O
வினைகள்
கோபால்ட்(II) ஆக்சைடு கனிம அமிலங்களுடன் வினைபுரிந்து தொடர்புடைய கோபால்ட் உப்புகளை உருவாக்குகிறது.
- CoO + 2 HX → CoX2 + H2O
பயன்பாடுகள்
பல நூற்றாண்டுகளாக மட்பாண்டத் தொழிலில் வண்ணமூட்டும் முகவராகக் கோபால்ட்(II) ஆக்சைடு பயன்படுத்தப்படுகிறது. இக்கூட்டுப்பொருள் ஆழ்ந்த நீல நிறத்தை (கோபால்ட் நீலம்) வழங்குகிறது. கோபால்ட்(II) ஆக்சைடின் பட்டை இடைவெளி சுமார் 2.4 எலக்ட்ரான் வோல்ட் ஆகும் கோபால்ட் நீலக் கண்ணாடிகளிலும் இது பயன்படுத்தப்படுகிறது.
மேற்கோள்கள்
- Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. பன்னாட்டுத் தரப்புத்தக எண்:0-07-049439-8. http://books.google.com/?id=Xqj-TTzkvTEC&pg=PA119. பார்த்த நாள்: 2009-06-06.
- Advanced Search – Alfa Aesar – A Johnson Matthey Company. Alfa.com. Retrieved on 2011-11-19.
- "Safety (MSDS) data for cobalt oxide". The Physical and Theoretical Chemistry Laboratory, Oxford University. பார்த்த நாள் 2008-11-11.
- Kannan, R.; Seehra, Mohindar S. (1987). "Percolation effects and magnetic properties of the randomly diluted fcc system CopMg1-pO". Physical Review B 35 (13): 6847. doi:10.1103/PhysRevB.35.6847.
- Silinsky, P. S.; Seehra, Mohindar S. (1981). "Principal magnetic susceptibilities and uniaxial stress experiments in CoO". Physical Review B 24: 419. doi:10.1103/PhysRevB.24.419.
- US 4389339, "Process for making a cobalt oxide catalyst"
- Kern, S. (1876). J. Chem. Soc.: 880.