இரேனியம் மூவாக்சைடு
இரேனியம் மூவாக்சைடு (Rhenium trioxide) என்பது ReO3 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட கனிம வேதியியல் சேர்மமாகும். இச்சேர்மம் இரேனியம் டிரையாக்சைடு, இரேனியம்(VI) ஆக்சைடு என்ற பெயர்களாலும் அழைக்கப்படுகிறது. உலோகத்தின் பளபளப்புடன் சிவப்பு நிறத் திண்மமாக தோற்றத்தில் தாமிரம் போல இது காட்சியளிக்கிறது. ஏழாவது குழு தனிமங்களில் (Mn, Tc, Re) நிலைப்புத்தன்மை கொண்ட ஒரே மூவாக்சைடு இரேனியம் மூவாக்சைடு ஆகும்.
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
இரேனியம் டிரையாக்சைடு | |||
| வேறு பெயர்கள்
இரேனியா, | |||
| இனங்காட்டிகள் | |||
| 1314-28-9 | |||
| EC number | 215-228-8 | ||
InChI
| |||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 102110 | ||
SMILES
| |||
| பண்புகள் | |||
| ReO3 | |||
| வாய்ப்பாட்டு எடை | 234.205 கி/மோல் | ||
| தோற்றம் | ஆழ்ந்த சிவப்பு நிறப் படிகங்கள் | ||
| அடர்த்தி | 6.92 கி/செ.மீ3 | ||
| உருகுநிலை | |||
காந்த ஏற்புத்திறன் (χ) |
+16.0•10−6 செ.மீ3/மோல் | ||
| ஒளிவிலகல் சுட்டெண் (nD) | 1.68 | ||
| கட்டமைப்பு | |||
| படிக அமைப்பு | கனசதுரம், cP4 | ||
| புறவெளித் தொகுதி | Pm3m, SpaceGroup = 221 | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| | |||
| Infobox references | |||
தயாரிப்பு
இரேனியம்(VII) ஆக்சைடை கார்பனோராக்சைடு கொண்டு ஒடுக்குவதன் மூலம் இரேனியம் மூவாக்சைடைத் தயாரிக்கலாம்[1]
- Re2O7 + CO → 2 ReO3 + CO2.
இரேனியம்(VII) ஆக்சைடை டையாக்சேனைப் பயன்படுத்தியும் ஒடுக்கி இதைத் தயாரிக்கிறார்கள் [2].
கட்டமைப்பு
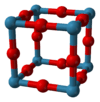
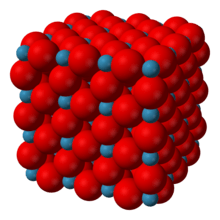
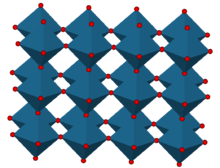
தொடக்கநிலை கனசதுர அலகுக் கூடாக இரேனியம் ஆக்சைடு படிகமாகிறது. 3.742 Å அல்லது 374.2 பைக்கோ மீட்டர் என்ற அணிக்கோவை அளவுருக்களை இப்படிகம் பெற்றுள்ளது. மேலும், அலகுக்கூட்டின் மையத்தில் பெரிய A நேர்மின் அயனி இடம்பெறாத பெரோவ்சிகைட்டின் கட்டமைப்பை ஒத்ததாகவும் இரேனியம் மூவாக்சைடின் கட்டமைப்பு உள்ளது. ஒவ்வொரு இரேனிய மையமும் ஆறு ஆக்சிசன் மையங்களால் ஆன எண்முக முக்கோணகத்தால் சூழப்பட்டுள்ளன. இந்த எண்முக முக்கோணகம் முப்பரிமாண கட்டமைப்பாக உருவாக மூலைகளைப் பகிர்ந்து கொள்கின்றன. ஒவ்வொரு ஆக்சிசன் அணுவும் இரண்டு அண்டை இரேனியம் அணுக்களை பெற்றிருப்பதால் இதில் ஆக்சிசனின் ஒருங்கிணைவு எண் 2 ஆகும் [3].
பண்புகள்
வெற்றிடத்தில் 400 பாகை செல்சியசு வெப்பநிலைக்குச் சூடுபடுத்தினால் இது விகிதச்சமமின்றி பிரிகையடைகிறது :[2]
- 3 ReO3 → Re2O7 + ReO2.
- 3 ReO3 → Re2O7 + ReO2
ஆக்சைடுகளில் வழக்கத்திற்கு மாறான ஓர் ஆக்சைடாக இரேனியம் மூவாக்சைடு திகழ்கிறது. ஏனெனில் இது மிக குறைவான மின் தடையைக் கொடுக்கிறது. வெப்பநிலை குறைவதற்கேற்ப இதன் மின்தடையும் குறைந்து ஒரு உலோகம் போன்ற பண்பை வெளிப்படுத்துகிறது. 300 கெல்வின் வெப்பநிலையில் இதன் மின் தடை 100.0 nΩ•m, ஆகும். அதேபோல 100 கெல்வின் வெப்பநிலையில் இதன் மின் தடை 6.0 nΩ•m ஆகக் குறைகிறது. இந்த அளவு கிட்டத்தட்ட 17 மடங்கு குறைவாகும் [3].
பயன்கள்
அமைடு ஒடுக்க கரிமத் தொகுப்பு வினைகளில் இரேனியம் மூவாக்சைடு சில பயன்களை அளிக்கின்றது [4].
மேற்கோள்கள்
- H. Nechamkin, C. F. Hiskey, "Rhenium(VI): Oxide (Rhenium Trioxide)" Inorganic Syntheses, 1950 Volume 3, pp. 186-188. எஆசு:10.1002/9780470132340.ch49
- G. Glemser "Rhenium (VI) Oxide" Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 2. p. 1482.
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ). Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண்:0080379419., p. 1047.
- Nishimura, Shigeo (2001). Handbook of Heterogeneous Catalytic Hydrogenation for Organic Synthesis (1st ). Newyork: Wiley-Interscience. பக். 408. பன்னாட்டுத் தரப்புத்தக எண்:9780471396987. https://books.google.com/books?id=RjZRAAAAMAAJ&q=0471396982&dq=0471396982&hl=en&sa=X&ei=BCacVMTgN5LmoASd34KQCQ&ved=0CB8Q6AEwAA.