மூலக்கூற்று வாய்பாடு
வேதியியல் வாய்ப்பாடு (Chemical formula) என்பது ஒரு குறிப்பிட்ட வேதிச் சேர்மம் அல்லது மூலக்கூறில் இடம்பெற்றுள்ள அணுக்களின் வேதியியல் விகிதங்கள் பற்றிய தகவல்களை கூறுகின்ற ஒரு வழிமுறையாகும். தனிமங்களின் வேதியியல் குறியீடுகள், எண்கள், அடைப்புக் குறிகள், கூட்டல் மற்றும் கழித்தல் குறிகள், காற்புள்ளிகள், கோடுகள் போன்றவை இவ்வழிமுறையில் பயன்படுத்தப்படுகின்றன. கீழொட்டு மற்றும் மேலொட்டுகள் உள்பட குறியீடுகளை ஓர் அச்சு வரியில் அச்சிடும் முறைக்கு இது கட்டுப்படுத்தப்படுகிறது. மூலக்கூறு வாய்ப்பாடு என்றும் இதை அழைக்கிறார்கள். வேதி வாய்ப்பாடு என்பது ஒரு பெயரல்ல. இதில் சொற்களுக்கு இடமில்லை. ஒரு வேதியியல் வாய்ப்பாடு சில எளிய இரசாயன கட்டமைப்புகளைக் குறிக்கலாம் என்றாலும், இது முழுமையான இரசாயன கட்டமைப்பு வாய்ப்பாடு போன்றது அல்ல.வேதிப்பொருள்கள் மற்றும் மூலக்கூறுகளின் எளிய அமைப்பையே வேதிவாய்ப்பாடுகள் வெளிப்படுத்துகின்றன. வேதிப் பெயர்கள் மற்றும் கட்டமைப்பு வாய்ப்பாடுகள் போன்றவற்றைக் காட்டிலும் வேதி வாய்ப்பாடுகளின் எல்லைகள் அதிகமாகக் கட்டுப்படுத்தப்படுகின்றன. ஒரு சேர்மத்தின் எடையை கணிப்பதற்கும் அச்சேர்மத்தின் மூலக்கூற்று வாய்பாடே பயன்படுகிறது.[1]
| அலுமினியம் சல்பேட்டு இன் மூலக்கூற்று வாய்ப்பாடு Al2(SO4)3 ஆகும். அலுமினியம் எக்சாடெக்கா ஐதரேட்டு Al2(SO4)3•16H2O என்று குறிக்கப்படுகிறது. |
| பியூட்டேனின் கட்டமைப்பு வாய்ப்பாடு. இது வேதி வாய்ப்பாடு அல்ல. பியூட்டேனின் பல்வேறு வாய்ப்பாடுகள் வருமாறு அனுபவ வாய்ப்பாடு: C2H5, மூலக்கூற்று வாய்ப்பாடு: C4H10 மற்றும் அரை கட்டமைப்பு வாய்ப்பாடு: CH3CH2CH2CH3. |
அனுபவ வாய்ப்பாடு என்பது ஓர் எளிய வகையான குறியீட்டு முறையாகும். இம்முறையில் எழுதப்படும் வாய்ப்பாடானது சேர்மத்தில் அல்லது மூலக்கூறிலுள்ள அணுக்களின் எண்ணியல் விகிதங்களை எழுத்துக்கள் மற்றும் எண்களை மட்டும் பயன்படுத்தி எழுதப்படுகிறது. மூலக்கூற்று வாய்ப்பாட்டில் ஒரு மூலக்கூறில் உள்ள அணுக்களின் எண்ணிக்கையை மட்டும் தெரிவிக்கின்றன. கட்டமைப்பைக் குறித்து இவை எதையும் தெரிவிப்பதில்லை. உதாரணமாக குளுக்கோசின் அணுபவ வாய்ப்பாடு CH2O ஆகும். கார்பன், ஆக்சிசன் அணுக்களின் எண்ணிக்கையைப் போன்று இரு மடங்கு ஐதரசன் அணுக்கள் குளுக்கோசில் உள்ளதை இவ்வாய்ப்பாடு தெரிவிக்கின்றது. ஆனால் குளுக்கோசின் மூலக்கூற்று வாய்ப்பாடு C6H12O6 என எழுதப்படுகிறது. 12 ஐதரசன் அணுக்கள், 6 கார்பன் அணுக்கள், 6 ஆக்சிசன் அணுக்கள் சேர்ந்தது குளுக்கோசு என்ற விளக்கத்தை மூலக்கூற்று வாய்ப்பாடு கூறுகிறது.
வேதிவாய்ப்பாட்டை அமுக்கப்பட்ட வாய்ப்பாடாக அல்லது அமுக்கப்பட்ட மூலக்கூற்று வாய்ப்பாடாக எழுதுவது சிக்கலை உண்டாக்குகிறது. இதை சில சந்தர்ப்பங்களில் அரை கட்டமைப்பு வாய்ப்பாடு என்கிறார்கள். அணுக்கள் சில குறிப்பிட்ட வழிகளைப் பின்பற்றி வேதியியல் ரீதியாக எவ்வாறு பிணைக்கப்பட்டுள்ளன என்பதை கூடுதல் தகவலாக இவ்வாய்ப்பாடு அளிக்கிறது, சகப்பிணைப்பு, அயனிப் பிணைப்பு அல்லது இந்த வகையான பல்வேறு பிணைப்புகள் குறித்த தகவல்கள் இதன் மூலம் அறியப்படுகின்றன. குறிப்பிட்டதொரு பிணைப்பை ஒற்றைப் பரிமாணத்தில் வெளிப்படுத்த இம்முறை உதவுகிறது. உதாரணமாக எத்தனாலின் அமுக்க வாய்ப்பாடு CH3-CH2-OH அல்லது CH3CH2OH ஆகும். இருப்பினும் இத்தகைய அமுக்க வாய்ப்பாடுகளும் அத்தியாவசியமாகக் கட்டுப்படுத்தப்படுகின்றன. அணுக்களுக்கு இடையிலான அணைவு பிணைப்புகளைக் குறிப்பிட, குறிப்பாக நான்கு அல்லது அதற்கு மேர்பட்ட பதிலிகளுடன் இணைகின்ற போது இத்தகைய கட்டப்பாடுகள் அவசியமாகிறது.
ஒரு வேதியியல் வாய்ப்பாட்டை ஓர் ஒற்றை வரியில் வேதியியல் குறியீடாக வெளிப்படுத்தப்பட வேண்டும் என்பதால் அது பெரும்பாலும் கூடுதல் விவரங்களை தரவியலாத ஒன்றாக இருக்கும். ஆனால் ஒரு கட்டமைப்பு வாய்ப்பாடு என்பது உண்மையான கட்டமைப்பை விளக்கும் வாய்ப்பாடாகவும் இரசாயன சேர்மங்களில் உள்ள அணுக்களுக்கு இடையில் நிலவும் வெளி சார்ந்த உறவின் ஒரு வரைகலைப் பிரதிநிதித்துவமாகவும் இருக்கும். பியூட்டேனின் கட்டமைப்பு மற்றும் வேதியியல் வாய்ப்பாடுகள் அருகில் கொடுக்கப்பட்டுள்ளன. கட்டமைப்பிலுள்ள பெரும் சிக்கல் காரணமாக குளுக்கோசை குறிப்பிட்டுச் சொல்லும் அரை கட்டமைப்பு வாய்ப்பாடு அல்லது அமுக்க வாய்ப்பாடு ஏதுமில்லை. ஏனெனில் குளுக்கோசின் வாய்ப்பாடான C6H12O6 என்பது பிரக்டோசு மற்றும் மானோசு ஆகியன்வற்ரையும் குறிக்கிறது. சிக்கலான கட்டமைப்பு வாய்ப்பாட்டைக் குறிப்பிட்டுச் சொல்லக்கூடிய நேரியல் இணை வேதிப் பெயர்கள் உள்ளன. ஆனால் அத்தகைய பெயர்களில் தனிமங்களின் குறியீடுகள், எண்கள் மற்றும் எளிமையான அச்சுக்கலை குறியீடுகள் ஆகியவற்றைக் காட்டிலும் பல சொற்களை பயன்படுத்த வேண்டியுள்ளது. ஆனால் வேதிவாய்ப்பாடுகளில் எளிமையான ஒற்றை வரி இவற்றை வரையறுக்கின்றன.
வேதி வினைகள் மற்றும் வேதி மாற்றங்களை விளக்குகின்ற வேதிச் சமன்பாடுகளை எழுத வேதி வாய்ப்பாடுகள் பயன்படுகின்றன. இவ்வினைகளில் பயன்படுத்தும் போது முழுமையான விவரங்களுடன் கூடிய கட்டமைப்பு வாய்ப்பாட்டை பயன்படுத்த இயலாது. இங்கு அணுக்களின் எண்ணிக்கையும் மின் சுமைகளின் அளவும் மட்டுமே குறிப்பிட்டால் போதுமானதாக உள்ளது. இதன் மூலம் வேதிச்சமன்பாட்டுகளை சமப்படுத்துதல் அதனுடன் தொடர்புடைய கனக்கீடுகளை மேற்கொள்ளுதல் போன்ற செயற்பாடுகள் எளிமையாகிறது.
அடைக்கப்பட்ட மூலக்கூறுகளின் வாய்ப்பாடு
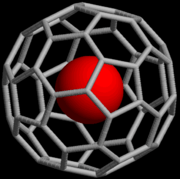
"@" வாய்ப்பாடு: M@C60
சில மூலக்கூறுகளும் அணுக்களும் சில வகை மூலக்கூறுகளில் அடைக்கப்பட்டு காணப்படும். அதாவது உள்ளேயுள்ள மூலக்கூறு அல்லது அணுவானது அதனைச் சூழவுள்ள மூலக்கூறுடல் வேதியல் பிணைப்பைப் பேணாமல் வெறுமனே அடைக்கப்பட்டுள்ளது. உதாரணமாக பக்மின்ஸ்டர்ஃபுலரின் (C60) மூலக்கூற்றில் அடைக்கப்பட்டுள்ள அணுவோடு (M) அம்மூலக்கூறின் வாய்ப்பாட்டை வழமையாக MC60 என்றே எழுதப்படும். எனினும் M உம் C60 உம் வேதியியல் தொடர்பைப் பேணாமை இவ்வாய்ப்பாட்டாற் காட்டப்படவில்லை. @ குறியீடைப் பயன்படுத்துவதால் இவை இரண்டும் வேதியியற் பிணைப்பைப் பேணவில்லை என்பதைக் காண்பிக்கலாம். அதாவது பக்மின்ஸ்டர்ஃபுலரினின் மூலக்கூற்று வாய்பாட்டை M@C60 என எழுத முடியும்.
இல் முறை
இல் முறை என்பது மூலக்கூறு வாய்ப்பாட்டை எழுதும் ஒரு முறையாகும். இங்கே கார்பனின் குறியீடு முதலாவதாகவும் பின்னர் ஐதரசன் குறியீடும் அதன் பின்னர் ஆங்கில நெடுங்கணக்கு வரிசையில் அணுக்களின் குறியீடுகளும் எழுதப்படுகின்றன. மூலக்கூறில் கார்பன் அணு இல்லாவிட்டால் நெடுங்கணக்கு வரிசையின் படி மூலக்கூறு வாய்ப்பாடு எழுதப்படும். இம்முறையானது மூலக்கூறு வாய்ப்பாட்டில் இலகுவாக அணு எண்ணிக்கைகளைத் தேடியறிய உதவும்.
1900ஆம் ஆண்டு எட்வின். ஏ. இல் என்பாரால் இம்முறை அறிமுகப்படுத்தப்பட்டது.[2] இதுவே மூலக்கூறு வாய்ப்பாடுகளை எழுதுவதில் அதிகமாகப் பயன்படுத்தப்படும் முறையாகும்.[3]
உதாரணங்கள்
பின்வரும் மூலக்கூற்று வாய்ப்பாடுகள் ஹில் முறையிலேயே எழுதப்பட்டுள்ளன:[3]
- BrH
- BrI
- CH3I
- C2H5Br
- H2O4S
மேற்கோள்கள்
- வேதியியல் தொகுதி-1, பதினொன்றாம் வகுப்பு, தமிழ் நாட்டுப் பாடநூல் கழகம், திருத்திய பதிப்பு 2007 பக்கம் 1.
- Edwin A. Hill (1900). "On a system of indexing chemical literature; Adopted by the Classification Division of the U.S. Patent Office". J. Am. Chem. Soc. 22 (8): 478–494. doi:10.1021/ja02046a005.
- Wiggins, Gary. (1991). Chemical Information Sources. New York: McGraw Hill. p. 120.
