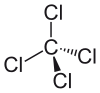
கார்பன் டெட்ராகுளோரைடு
கார்பன் டெட்ராகுளோரைடு (Carbon tetrachloride) என்பது ஒரு கரிம சேர்மம். இதன் மூலக்கூறு வாய்ப்பாடு CCl4. இது தீயணைப்பான்களிலும், குளிர்சாதனப் பெட்டிகளிலும் சுத்தம் செய்யப் பயன்படுகிறது. இது ஒரு நிறமற்ற, மணமுள்ள வாயு. இது சாதாரண வெப்பநிலையில் தீப்பற்றாது.
| |||
| பெயர்கள் | |||
|---|---|---|---|
| ஐயூபிஏசி பெயர்
கார்பன் டெட்ராகுளோரைடு,டெட்ரா குளோரோ மீத்தேன் | |||
| வேறு பெயர்கள்
பென்சீன் ஃபார்ம், கார்பன் குளோரைடு, கார்பன் டெட் , ஃபிரியான்-10,மீத்தேன் டெட்ராகுளோரைடு | |||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
| Infobox references | |||
வரலாறு
இச்சேர்மம் பிரெஞ்சு அறிவியல் அறிஞர் ஹென்றி விக்டர் ரெக்னால்ட்[1] என்பவரால் 1839-ல் கண்டறியப்பட்டது. இச்சேர்மம் கீழ்க்கண்ட வினையின் மூலம் உருவாகிறது.குளோரின் மற்றும் குளோரோஃபார்ம் இணைவதால் கார்பன் டெட்ராகுளோரைடு கிடைக்கிறது.
- CH4 + 4 Cl2 → CCl4 + 4 HCl
அமைப்பு
இச்சேர்மம் நான்கு குளோரின் மூலக்கூறுகளும், ஒரு கார்பன் அணுவும் கொண்டுள்ளது. இது நாற்பிணைப்பு கொண்டுள்ளது. கார்பன் அணுவுடன், நான்கு குளோரின் மூலக்கூறுகளும் சகப்பிணைப்புக் கொண்டுள்ளது. இது மீத்தேன் மூலக்கூறு போன்ற அமைப்பில் இருப்பதால் இதற்கு "ஹாலோ மீத்தேன் [2]" என்று அழைக்கப்படுகிறது.
பண்புகள்
இது ஒரு முனைவற்ற மூலக்கூறு, இது முனைவற்ற மூலக்கூறுகளையும், எண்ணெய் பொருள்களையும், கொழுப்பு பொருள்களையும் கரைக்கும். இது குளோரின் மூலக்கூறுகளின் மணத்துடன் இருக்கும்.
மேற்கோள்கள்
- V. Regnault (1839) "Sur les chlorures de carbone CCl et CCl2" (On the chlorides of carbon CCl and CCl2 ), Annales de Chimie et de Physique, vol. 70, pages 104-107. Reprinted in German as: V. Regnault (1839). "Ueber die Chlorverbindungen des Kohlenstoffs, C2Cl2 und CCl2". Annalen der Pharmacie 30 (3): 350–352. doi:10.1002/jlac.18390300310.
- F. Brezina, J. Mollin, R. Pastorek, Z. Sindelar. Chemicke tabulky anorganickych sloucenin (Chemical tables of inorganic compounds). SNTL, 1986.
| குளோரைடுகள் | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| HCl | He | ||||||||||||||||||
| LiCl | BeCl2 | BCl3 B2Cl4 |
CCl4 | NCl3 ClN3 |
Cl2O ClO2 Cl2O7 |
ClF ClF3 ClF5 |
Ne | ||||||||||||
| NaCl | MgCl2 | AlCl AlCl3 |
SiCl4 | P2Cl4 PCl3 PCl5 |
S2Cl2 SCl2 SCl4 |
Cl2 | Ar | ||||||||||||
| KCl | CaCl CaCl2 |
ScCl3 | TiCl2 TiCl3 TiCl4 |
VCl2 VCl3 VCl4 VCl5 |
CrCl2 CrCl3 CrCl4 |
MnCl2 | FeCl2 FeCl3 |
CoCl2 CoCl3 |
NiCl2 | CuCl CuCl2 |
ZnCl2 | GaCl2 GaCl3 |
GeCl2 GeCl4 |
AsCl3 AsCl5 |
Se2Cl2 SeCl4 |
BrCl | KrCl | ||
| RbCl | SrCl2 | YCl3 | ZrCl3 ZrCl4 |
NbCl4 NbCl5 |
MoCl2 MoCl3 MoCl4 MoCl5 MoCl6 |
TcCl4 | RuCl3 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl InCl2 InCl3 |
SnCl2 SnCl4 |
SbCl3 SbCl5 |
Te3Cl2 TeCl4 |
ICl ICl3 |
XeCl XeCl2 | ||
| CsCl | BaCl2 | HfCl4 | TaCl5 | WCl2 WCl3 WCl4 WCl5 WCl6 |
Re3Cl9 ReCl4 ReCl5 ReCl6 |
OsCl4 | IrCl2 IrCl3 IrCl4 |
PtCl2 PtCl4 |
AuCl AuCl3 |
Hg2Cl2, HgCl2 |
TlCl | PbCl2, PbCl4 |
BiCl3 | PoCl2, PoCl4 |
AtCl | RnCl2 | |||
| FrCl | RaCl2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| LaCl3 | CeCl3 | PrCl3 | NdCl2, NdCl3 |
PmCl3 | SmCl2, SmCl3 |
EuCl2, EuCl3 |
GdCl3 | TbCl3 | DyCl2, DyCl3 |
HoCl3 | ErCl3 | TmCl2 TmCl3 |
YbCl2 YbCl3 |
LuCl3 | |||||
| AcCl3 | ThCl4 | PaCl5 | UCl3 UCl4 UCl5 UCl6 |
NpCl4 | PuCl3 | AmCl2 AmCl3 |
CmCl3 | BkCl3 | CfCl3 | EsCl3 | Fm | Md | No | LrCl3 | |||||