அமோனியம் அறுகுளோரோபிளாட்டினேட்டு
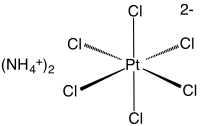
அமோனியம் அறுகுளோரோபிளாட்டினேட்டு (Ammonium hexachloroplatinate) என்பது (NH4)2[PtCl6] என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். இச்சேர்மம் அமோனியம் குளோரோபிளாட்டினேட்டு என்றும் அழைக்கப்படுகிறது. நீரில் கரையக்கூடிய பிளாட்டினம்(IV) வகை உப்பிற்கு இவ்வுப்பு ஓர் அரிய உதாரணமாகும். நீருறிஞ்சும் தன்மையில்லாத இச்சேர்மம் தண்ணீரில் முனைப்புடன் வினைபுரிந்து மஞ்சள் நிறக் கரைசலைக் கொடுக்கிறது. 1 மோலார் NH4Cl முன்னிலையில் அமோனியம் அறுகுளோரோபிளாட்டினேட்டின் கரைதிறன் 0.0028 கி/100 மி.லி மட்டுமேயாகும்.
 | |
2PtCl6Xray.tif.png) | |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
அமோனியம் அறுகுளோரோபிளாட்டினேட்டு(IV) | |
| வேறு பெயர்கள்
அமோனியம் குளோரோபிளாட்டினேட்டு | |
| இனங்காட்டிகள் | |
| 16919-58-7 | |
| ChEBI | CHEBI:59604 |
| ChemSpider | 10628022 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
SMILES
| |
| பண்புகள் | |
| (NH4)2PtCl6 | |
| வாய்ப்பாட்டு எடை | 443.87 கி/மோல் |
| தோற்றம் | மஞ்சள் நிறப் படிகங்கள் |
| மணம் | நெடியற்றது |
| அடர்த்தி | 3.065 கி/செ.மீ3 |
| உருகுநிலை | |
| 0.289 கி/100மி.லி (0 °செC) 0.7 கி/100மி.லி (15 ° செ)[1] 0.499 கி/100மி.லி (20 °செ) 3.36 கி/100மி.லி (100 °செ) | |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
தயாரிப்பு மற்றும் அமைப்பு
தனித்தனியாக நான்முக அமோனியம் நேர்மின் அயனிகளையும் எண்முக [PtCl6]2− எதிர்மின் அயனிகளையும் இச்சேர்மம் கொண்டிருக்கிறது. பொதுவாக, அறுகுளோரோ பிளாட்டினிக் அமிலத்துடன் ஒரு அமோனியம் உப்புக் கரைசலைச் சேர்த்து மெல்லிய மஞ்சள் நிற அமோனியம் அறுகுளோரோபிளாட்டினேட்டு தயாரிக்கப்படுகிறது.[2] இந்த அணைவுச் சேர்மம் மிகக் குறைவாகக் கரைவதால், தாதுக்களில் இருந்தும் மறுசுழற்சிக் கசடுகளிலிருந்தும் பிளாட்டினத்தைத் தனித்துப் பிரித்தெடுக்க இச்சேர்மம் பயன்படுத்தப்படுகிறது.[3]
புளோரைட்டு அமைப்பை ஒத்த கனசதுர நோக்குருவில் இச்சேர்மம் படிகமாவதாக எக்சு கதிர் படிகவியல் ஆய்வுகள் தெரிவிக்கின்றன. [PtCl6]2- மையங்கள் எண்முக வடிவிலும் அமோனியம் மையங்கள் குளோரைடு ஈந்தணைவிகளுடன் ஐதரசன் பிணைப்புடனும் காணப்படுகின்றன.[4]
பயன்கள் மற்றும் வினைகள்
பிளாட்டின முலாம் பூசுவதற்கு அமோனியம் அறுகுளோரோபிளாட்டினேட்டு பயன்படுகிறது. இதை ஐதரசன் வாயுப் பாய்மத்தில் 200 பாகை செல்சியசு வெப்பநிலைக்குச் சூடாக்கும் போது புரை பிளாட்டினம் உருவாகிறது. இதனுடன் குளோரின் சேர்த்து சூடாக்கினால் H2PtCl6 உருவாகிறது.[2]
மேற்கோள்கள்
- "ammonium hexachloroplatinate(IV)". Chemister.ru (2007-03-19). பார்த்த நாள் 2014-06-03.
- George B. Kauffman (1967). "Ammonium Hexachloroplatinate(IV)". Inorganic Syntheses. Inorganic Syntheses 9: 182–185. doi:10.1002/9780470132401.ch51. பன்னாட்டுத் தரப்புத்தக எண்:978-0-470-13240-1.
- Cotton, S. A. Chemistry of Precious Metals, Chapman and Hall (London): 1997. ISBN 0-7514-0413-6.
- Verde-Gómez, Y.; Alonso-Nuñez, G.; Cervantes, F.; Keer, A. "Aqueous solution reaction to synthesize ammonium hexachloroplatinate and its crystallogrpahic and thermogravimetric characterization" Materials Letters, 2003, volume 57, p 4667-4672. எஆசு:10.1016/S0167-577X(03)00381-1