அலுமினியம் செலீனைடு
அலுமினியம் செலீனைடு (Aluminium selenide) என்பது Al2Se3. என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும்
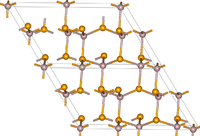 | |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
அலுமினியம்(III) செலீனைடு | |
| இனங்காட்டிகள் | |
| 1302-82-5 | |
| ChemSpider | 144477 |
| EC number | 215-110-6 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 164804 |
SMILES
| |
| பண்புகள் | |
| Al2Se3 | |
| வாய்ப்பாட்டு எடை | 290.84 கி/மோல் |
| தோற்றம் | மஞ்சளும் பழுப்பும் கலந்த நிறத்துகள் |
| மணம் | நெடியற்றது |
| அடர்த்தி | 3.437 கி/செ.மீ3 |
| உருகுநிலை | |
| சிதைவடையும் | |
| கட்டமைப்பு | |
| படிக அமைப்பு | ஒற்றச்சரிவு, mS20, இடக்குழு Cc, No. 9[2] |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
-566.9 கி.யூ/மோல் |
| நியம மோலார் எந்திரோப்பி S |
154.8 யூ/மோல் கெ |
| தீங்குகள் | |
| ஈயூ வகைப்பாடு | பட்டியலிடப்படவில்லை |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
தயாரிப்பு
அலுமினியம் மற்றும் செலீனியம் சேர்ந்த கலவையை 1000 0 செல்சியசு வெப்பநிலையில் எரியூட்டுவதால் இத்திண்மம் தயாரிக்கப்படுகிறது.
- 2 Al + 3 Se → Al2Se3
தூய்மையான நிலையில் இது வெண்மை நிறத்துடன் காணப்படுகிறது. சில குறிப்பிட்ட மாதிரிகள் வண்ணங்களிலும் அறியப்படுகின்றன[3]. அலுமினியம் செலினைடு மாதிரிகளை ஈரப்பதத்தில் இருந்து விலக்கி பாதுகாப்பாக வைக்க வேண்டும். ஏனெனில் இது உடனடியாக நீராற்பகுப்புக்கு உட்பட்டு அபாயகரமான வாயுவான ஐதரசன் செலினைடு வாயுவை வெளியிடுகிறது.:[4]
- Al2Se3 + 3 H2O → Al2O3 + 3 H2Se
பயன்கள்
ஐதரசன் செலீனைடு வாயுவை தயாரிப்பதற்கான முன்னோடிச் சேர்மமாக அலுமினியம் செலீனைடு விளங்குகிறது. இந்த திண்மநிலை சேர்மத்துடன் அமிலங்களைச் சேர்க்கும் போது ஐதரசன் செலீனைடு உண்டாகிறது.
பாதுகாப்பு
அலுமினியம் செலீனைடை ஈரம் மற்றும் காற்று படாமல் பாதுகாப்பாகக் கையாள வேண்டும்.
மேற்கோள்கள்
- Lide, David R. (1998). Handbook of Chemistry and Physics (87 ). Boca Raton, FL: CRC Press. பக். 4–40. பன்னாட்டுத் தரப்புத்தக எண்:0-8493-0594-2
- Steigmann, G. A.; Goodyear, J. (1966). "The crystal structure of Al2Se3". Acta Crystallographica 20: 617. doi:10.1107/S0365110X66001506.
- Waitkins, G. R.; Shutt, R. (1946). "Aluminum Selenide and Hydrogen Selenide". Inorganic Syntheses 2: 183–186. doi:10.1002/9780470132333.ch55.
- Bernd E. Langner "Selenium and Selenium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. எஆசு:10.1002/14356007.a23_525.