ஆஃபினியம்
ஆஃபினியம் (Hafnium; ஆஃபினியம்; /HAF-nee-əm) , Hf என்னும் குறியீடு கொண்ட வேதியியல் தனிமம். இதன் அணுவெண் 72. இதன் அணுக்கருவில் 106 நொதுமிகள் (நியூட்ரான்கள்) உள்ளன. இது பிறழ்வரிசை மாழைகள் வரிசையைச் சேர்ந்த, வெள்ளி போல் வெண்சாம்பல் நிறமுடைய, சிர்க்கோனியத்தைப் போன்ற வேதியியல் பண்புகள் கொண்ட ஒரு தனிமம். இதனை டென்மார்க்கில் உள்ள கோப்பனாகன் என்னும் இடத்தில் கண்டுபிடித்ததால், கோப்பனாகனின் இலத்தீன் பெயராகிய ஃகாவ்னியா (Hafnia) என்பதில் இருந்து இப்பெயர் பெற்றது. திமீத்ரி மென்டெலீவ் இப்படி ஒரு தனிமம் இருக்க வேண்டும் என்று இதனைக் கண்டுபிடிக்கும் முன்பே 1869 இல் முற்கூறினார்.
| ஆஃபினியம் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
72Hf | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| தோற்றம் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
சாம்பல் நிறம் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பொதுப் பண்புகள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பெயர், குறியீடு, எண் | ஆஃபினியம், Hf, 72 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| உச்சரிப்பு | /ˈhæfniəm/ HAF-nee-əm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| தனிம வகை | பிறழ்வரிசை மாழை | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| நெடுங்குழு, கிடை வரிசை, குழு | 4, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| நியம அணு நிறை (அணுத்திணிவு) |
178.49 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
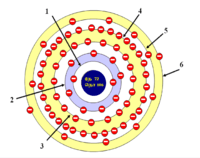
| இலத்திரன் அமைப்பு | [Xe] 4f14 5d2 6s2 2, 8, 18, 32, 10, 2  Electron shells of Hafnium (2, 8, 18, 32, 10, 2) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| இயற்பியற் பண்புகள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| நிலை | திண்மம் | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அடர்த்தி (அ.வெ.நிக்கு அருகில்) | 13.31 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| திரவத்தின் அடர்த்தி உ.நி.யில் | 12 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| உருகுநிலை | 2506 K, 2233 °C, 4051 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| கொதிநிலை | 4876 K, 4603 °C, 8317 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| உருகலின் வெப்ப ஆற்றல் | 27.2 கி.யூல்·மோல்−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வளிமமாக்கலின் வெப்ப ஆற்றல் | 571 கி.யூல்·மோல்−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வெப்பக் கொண்மை | 25.73 யூல்.மோல்−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ஆவி அழுத்தம் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அணுப் பண்புகள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ஒக்சியேற்ற நிலைகள் | 4, 3, 2 (இருவினை ஆக்சைடு) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மின்னெதிர்த்தன்மை | 1.3 (பாலிங் அளவையில்) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மின்மமாக்கும் ஆற்றல் | 1வது: 658.5 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2வது: 1440 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3வது: 2250 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| அணு ஆரம் | 159 பிமீ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பங்கீட்டு ஆரை | 175±10 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பிற பண்புகள் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| படிக அமைப்பு | அறுகோணப்பட்டகம் | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| காந்த சீரமைவு | சிற்றிசைவு காந்தவியல்[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மின்கடத்துதிறன் | (20 °C) 331 nΩ·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வெப்ப கடத்துத் திறன் | 23.0 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| வெப்ப விரிவு | (25 °C) 5.9 µm·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ஒலியின் வேகம் (மெல்லிய கம்பி) | (20 °C) 3010 மீ.செ−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| யங் தகைமை | 78 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| நழுவு தகைமை | 30 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பரும தகைமை | 110 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பாய்சான் விகிதம் | 0.37 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மோவின் கெட்டிமை (Mohs hardness) |
5.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| விக்கெர் கெட்டிமை | 1760 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| பிரிநெல் கெட்டிமை | 1700 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS எண் | 7440-58-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| மிக உறுதியான ஓரிடத்தான்கள் (சமதானிகள்) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| முதன்மைக் கட்டுரை: ஆஃபினியம் இன் ஓரிடத்தான் | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ஆஃபினியம், மின்கருவி முனைகளிலும், இழைகளிலும் பயன்படுகின்றது. 21 ஆம் நூற்றாண்டு நானோ நுண்மின்கருவிகளில், 45 நானோ.மீ நீளத்துக்கும் குறைவான இடைக்கால் உள்ள தொகுசுற்றுகளில், ஃகாவ்னியத்தின் ஆக்சைடு, சிலிக்கேட்டு போன்றவை சிலிக்கான்-டை-ஆக்சைடிற்கு ஒரு மாற்றாகப் பயன்படத் தொடங்கியுள்ளது, நியோபியம், டைட்டேனியம், தங்குசிட்டன் போன்றாவற்றோடு சில கலப்பு மாழைகளில் (கலப்புலோகங்களில்)பயன்படுகின்றது.
ஆஃபினியம், நொதுமிகளை (நியூட்ரான்களை)ப் பிடிப்பதில் அல்லது உள்வாங்குவதில் அதிகத் திறன் (பிடிதிறன், capture cross section) கொண்டதால், அணுவுலைகளில் கட்டுப்பாட்டு எரிகோல்களில் பயன்படுத்தப் படுகின்றது.
பண்புகள்
இயற்பியல் பண்புகள்

ஆஃபினியம் வெள்ளிபோல் பளபளப்பான, வெண்சாம்பல் நிறமுடைய தட்டிகொட்டி வடிவம் மாற்றக்கூடிய, அரிப்பெதிர்ப்புத் தன்மை கொண்ட பொருள். சிர்க்கோனியத்தை போன்ற பண்புகள் கொண்டது (இதைப்போலவே பிணைவு எதிர்மின்னிகள் அமைப்புக் கொண்டதால்). இதன் இயற்பியல் பண்புகள் சிர்க்கோனியக் கலப்பால் பெரிதும் மாறக்கூடியது, குறிப்பாக அணுவுலைப் பயன்பாடுகளில். [2]
ஆஃப்னியத்தின் அடர்த்தி சிர்க்கோனியத்தின் அடர்த்தியைப் போல் ஏறத்தாழ இருமடங்காகும். உயர்வெப்ப நொதுமிகளைப் பிடிப்பதில் திறம் மிக்கது. இதை ஒப்பிடும்பொழுது சிர்க்கோனியம் நொதுமிகளை எளிதாக ஊடுகடத்துவது.
வேதியியல் பண்புகள்
_oxide.jpg)
காற்றில் இருந்தால் ஆஃபினியம் வேதியியல் வினைப்பாட்டால் ஒருவகையான காப்புப் படலம் உருவாக்கிக்கொள்கின்றது, இத் தடுப்புப் படலத்ததல் மேற்கொண்ட அரிப்பில் இருந்து காப்பு ஏற்படுகின்றாது, ஆனால் மிகவும் பொடியாக இருக்கும் ஆஃபினியம், சிர்க்கோனியம் போலவே காற்றில் தன்னியல்பாய் உடனே தீப்பற்றும் பண்புடையது. தீ கக்குவது போலவோ, தீ நாக்குகள் பரவுவது போலவோ காட்டும் சில நெருப்புத்தீ உண்டாக்கும் விளையாட்டு நுட்பங்களில் சிர்க்கோனியம் பயன்படுவது போல இதனையும் பயன்படுத்தலாம்.[3] இம் மாழை (உலோகம்) வேதியியல் செறிந்த ஆல்க்கலிகளாலும் அதிகம் தாக்கம் பெறாதது
ஆஃப்னியத்தின் வேதியியல் பண்புகள் சிர்க்கோனியத்துடன் மிகவும் நெருக்கமானது. வேதியியல் வினையைக் கொண்டு ஒன்றில் இருந்து மற்றொன்றைப் பிரித்தறிதல் கூட சற்றுக் கடினம். உருகுநிலை, கொதிநிலை, கரைப்பான்களில் கரைமை, அடர்த்தி ஆகியவையே சிர்க்கோனியத்தையும் ஃகாவ்னியத்தையும் வேறுபடுத்திக்காட்டும் எளிய கூறுகள் [4]
கிடைப்பு

ஆஃபினியம் தனிமம் புவியின் மேலோட்டுப் பகுதியில் (புறணியில்) எடையளவாகக் கண்டால் மில்லியன் பகுதியியில் 5.8 பகுதிகள் (5.8 மிபப) என்னும் விகிதத்தில் மிகவும் சிறிதளவாகவே உள்ளது என்று கணித்துள்ளார்கள். இயற்கையில் தனியாக தனிமமாகக் கிடைப்பதில்லை. ஆனால் சிர்க்கோன் (ZrSiO4, ) போன்ற கனிமங்களில் சிர்க்கோனியம் தனிமம் கலந்திருக்கும் கனிமங்களில் பெரும்பாலும் காணப்படுகின்றது. இக் கனிமங்களில் சிர்க்கோனியத்துக்கு மாற்றாக 1 – 4 % ஆஃபினியம் கலந்திருக்கும். மிக அரிதாகவே படிகங்களாகும் பொழுது ஆஃபினியம்/சிர்க்கோனியம் விகிதம் மாறுபடுகின்றது, இதனால் சிர்க்கோனியத்தை விடக் கூடுதலாக ஆஃபினியம் (Hf > Zr) உள்ள, ஆனால் ஒரேபடிகவடிவம் கொண்ட, கனிமமாக ஆஃபினான் ('hafnon') (Hf,Zr)SiO4) என்னும் கனிமம் அறியப்படுகின்றது [5] An old (obsolete) name for a variety of zircon containing unusually high Hf content is alvite.[6]
சிர்க்கோனியமும் (எனவே ஆஃபினியமும்) பெருமளவில் கிடைக்கும் இடங்கள் . பிரேசிலும் ஆப்பிரிக்காவில் உள்ள மலாவியும் மேற்கு ஆத்திரேலியாவும் ஆகும். பிரேசிலிலும், மலாவியிலும் கிடைக்கும் கனிம மணலும், பெகுமாட்டைட்டு (pegmatite) என்னும் தீப்பாறைகளும், மேற்கு ஆத்திரேலியாவில் வெல்டு மலை என்னும் இடத்தில் உள்ள கிரௌன் பாலிமெட்டாலிக் படிவில் கிடைக்கும் கார்போனட்டைட்டு என்னும் கனிமமும் முகனையானவை (முக்கியமானவை). ஆத்திரேலியாவில் நியூ சவுத்வேல்சு என்னும் மாநிலத்தில் உள்ள இடபோ என்னும் இடத்தில் உள்ள சிர்க்கோனியம்-ஆஃபினியம் சிலிக்கேட்டுக் கனிமங்கள் யூடியாலைட்டு (eudialyte), ஆர்ம்சிட்ராங்கைட்டு (armstrongite) ஆகியவையும் இத்தனிமம் பெறத்தக்கதாக இருக்கும் கனிமம் என்று கருதப்படுகின்றது[7]. இசுகாண்டிநேவியாவில் கிடைக்கும் தோர்ட்வைட்டைட்டு (Thort Veittite) என்னும் கனிமபொருள் சிர்க்கோனியத்தைவிட அதிக அளவு ஆஃபினியம் கொண்டிருக்கின்றது[8]
மக்கள் தொகை கூடக்கூட, இதன் தேவைகள் பெருகினால் ஆஃபினியம் 10 ஆண்டுகள் வரை மட்டுமே கிடைக்கும் என்று கணித்திருக்கின்றறர்கள்[9].
உற்பத்தி

தைட்டேனியம் (Ti) உள்ள கனிமங்களாகிய இல்மெனைட்டு (ilmenite), இரூட்டைல் (rutile)ஆகியவை கொண்டிருக்கும் கனத்தக் கனிமமணற் பாறைப்படிவுகள் பெரும்பான்மையான சிர்க்கோனியத்தையும், அதனோடு இயல்பாக இருக்கும் ஆஃவினியத்தையும் தருகின்றது[10].
பல்வேறு கரைப்பான்களைக் கொண்டு, நீர்ம-நீர்ம பிரித்தெடுப்பு முறைவழி (Liquid-liquid extraction processes) ஆஃவினியத்தைப் பிரித்தெடுப்பது பரவலாகப் பயன்படுகின்றது.[11] ஆஃவினிய உற்பத்தியில் ஏறத்தாழ பாதியளவு சிர்க்கோனியத்தைத் தூய்மைப்படுத்துவதில் இருந்து கிடைக்கின்றது
மேற்கோள்களும் அடிக்குறிப்புகளும்
- Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics 81st edition, CRC press.
- Schemel, J. H. (1977). ASTM Manual on Zirconium and Hafnium. ASTM International. பக். 1–5. பன்னாட்டுத் தரப்புத்தக எண்:9780803105058. http://books.google.com/?id=dI_LssydVeYC.
- "Occupational Safety and Health Guideline for Hafnium". U.S. Department of Labor. பார்த்த நாள் 2008-09-10.
- Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils; (1985) (in German). Lehrbuch der Anorganischen Chemie (91–100 ). Walter de Gruyter. பக். 1056–1057. பன்னாட்டுத் தரப்புத்தக எண்:3110075113.
- Deer, William Alexander; Howie, R.A.; Zussmann, J. (1982). The Rock-Forming Minerals, volume 1A: Orthosilicates. Longman Group Limited. பக். 418–442. பன்னாட்டுத் தரப்புத்தக எண்:0582465265.
- Lee, O. Ivan (1928). "The Mineralogy of Hafnium". Chemical Reviews 5: 17. doi:10.1021/cr60017a002.
- "Dubbo Zirconia Project Fact Sheet" (PDF). Alkane Resources Limited (June 2007). மூல முகவரியிலிருந்து 2008-02-28 அன்று பரணிடப்பட்டது. பார்த்த நாள் 2008-09-10.
- அறிவியல் கலைக்களஞ்சியம், தொகுதி 19, தமிழ்ப் பல்கலைக்கழகம், தஞ்சாவூர், 2010
- cite web |url=http://www.science.org.au/nova/newscientist/ns_diagrams/027ns_005image2.jpg |title = New Scientist diagram How Long Will It Last
- Gambogi, Joseph. "Yearbook 2008: Zirconium and Hafnium" (pdf). United States Geological Survey. பார்த்த நாள் 2008-10-27.
- Hedrick, James B.. "Hafnium" (pdf). United States Geological Survey. பார்த்த நாள் 2008-09-10.