எத்தேன்
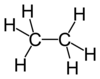
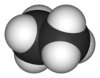
ஈத்தேன் (Ethane) என்பது C2H6 என்ற மூலக்கூற்று வாய்ப்பாட்டைக் கொண்ட கரிமச் சேர்மங்களைக் குறிக்கிறது. இதை எத்தேன் என்ற பெயராலும் அழைக்கிறார்கள். சாதாரணமான வெப்பநிலை மற்றும் அழுத்தத்தில் ஈத்தேன் நிறமற்ற மணமற்ற வாயுவாகக் காணப்படுகிறது. பிற ஐதரோ கார்பன்கள் போல ஈத்தேனும் இயற்கை வாயுவிலிருந்து பேரளவில் தொழிற்சாலைகளில் தனித்துப் பிரித்தெடுக்கப்படுகிறது. பெட்ரோலியத்தை சுத்திகரிப்பு செய்யும் போது பெட்ரோ வேதிப்பொருள்களுடன் உடன் விளைபொருளாகவும் கிடைக்கிறது. எத்திலீன் உற்பத்திக்குப் பயன்படுத்துவது ஈத்தேனின் முதன்மையான பயனாகக் கருதப்படுகிறது.
| ஈத்தேன் | |
|---|---|
  | |
| பொது | |
| வேதியியல் முறைப் பெயர் | எத்தேன் |
| பிற பெயர்கள் | டை-மெத்தில் dimethyl, எத்தில் ஐதரைடு மெத்தில்-மெத்தேன் |
| மூலக்கூறு சுருக்குத் தொடர் | C2H6 |
| SMILES | CC |
| InChI | InChI=1/C2H6 /c1-2/h1-2H3 |
| மூலக்கூறு பொருண்மம் | 30.07 கி/மோல் |
| தோற்றம் | நிறமற்ற வளிமம் |
| CAS எண் | [74-84-0] |
| கட்டமைப்பு | |
| Symmetry group | Staggered phase: D3d |
| பண்புகள் | |
| அடர்த்தி மற்றும் பொருளின் இயல்பு நிலை | 1.212 கி.கி/மீ3, வளிமம் |
| கரையும் திறன் நீரில் | 4.7 கி/100 மி.லி (? °C) |
| உருகு வெப்ப நிலை | -182.76 °செ (90.34 K) |
| கொதி வெப்ப நிலை | -88.6 °செ (184.5 K) |
| காடித்தன்மை காடித்திறன் (pKa) | 50 |
| கேடுகள் ஊறுகள் | |
| பொருள்களைப்பற்றிய காப்புத்தன்மை தாள், MSDS | External MSDS |
| EU classification | Highly flammable (F+) |
| என்.எப்.பி.ஏ 704 |
4
1
0
|
| R-சொற்றொடர்கள் | R12 |
| S-சொற்றொடர்கள் | (S2), S9, S16, S33 |
| தீப் பற்றும் நிலை, Flash point | -135 °செ |
| தானே தீப்பிடிக்கும் நிலை வெப்பநிலை |
472 °செ |
| வெடிக்கும் எல்லை | 3.0–12.5% |
| வேதிப்பொருள்களின் நச்சு விளைவுகளின் பதிவேடு number | KH3800000 |
| மேலதிக தரவுப் பக்கம் | |
| கட்டமைப்பும் & பண்புகளும் |
n, εr, etc. |
| வெப்ப இயங்கியல் தரவு |
நிலியின் தன்மை திண்மம், நீர்மம், வாயு |
| Spectral data | UV, IR, NMR, MS |
| தொடர்புடைய கூட்டணுக்கள் | |
| Related ஆல்க்கேன்s | மீத்தேன் புரொப்பேன் |
| தொடர்புடைய கூட்டணுக்கள் | எத்தனால் |
| மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த் நிலையில் (at 25°C, 100 kPa) இருக்கும் Infobox disclaimer and references | |
கட்டமைப்பில் உள்ள ஓர் ஐதரசன் அணுவை இடப்பெயர்ச்சி செய்துவிட்டு அதற்குப் பதிலாக வேரு வேதி வினைக்குழுவை மாற்றீடு செய்து ஈத்தேனுடன் தொடர்புடைய பிற சேர்மங்கள் தயாரிக்கப்படுகின்றன. ஈத்தேன் சேர்மத்தின் ஒரு பகுதிக் கூறு எத்தில் குழு என்ற வேதி வினைக்குழுவாக கருதப்படுகிறது. உதாரணமாக ஓர் எத்தில் குழுவுடன் ஐதராக்சில் குழு இனைக்கப்பட்டால் அச்சேர்மத்தை எத்தனால் என்கிறோம். இது மதுபானங்களில் உள்ள ஆல்ககால் ஆகும்.
வரலாறு
1834 ஆம் ஆண்டில் மைக்கேல் பாரடே என்பவரால் ஈத்தேன் முதன் முதலில் தயாரிக்கப்பட்டது. பொட்டாசியம் அசிட்டேட் கரைசலை மின்னாற்பகுப்புக்கு உட்படுத்தி இவர் ஈத்தேனைத் தயாரித்தார். இந்த வினையில் உருவான ஐதரோகார்பன் விளைபொருள் மீத்தேன் என்று இவர் தவறாகப் புரிந்து கொண்டார். இதனால் மேலும் இந்த சேர்மத்தை தொடர்ந்து ஆராயாமல் கைவிட்டார் [1]. 1847-1849 காலப்பகுதியில் கரிம வேதியியலின் இயங்குறுப்புத் தத்துவத்தை நிரூபிப்பதற்காக எர்மான் கோல்ப் மற்றும் எட்வர்ட்டு பிராங்க்லேண்டு ஆகியோர் எத்தில் சயனைடு [2] மற்றும் எத்தில் அயோடைடுடன் [3] பொட்டாசியம் தனிமத்தைச் சேர்த்து ஒடுக்கமடையச் செய்து ஈத்தேனை உருவாக்கினர். இதற்கு அவர்கள் பாரடே செய்ததைப் போல நீரிய அசிட்டேட்டுகளை மின்னாற்பகுப்புக்கு உட்படுத்தினர். இவர்களும் இவ்வினையில் விளைந்தது மீத்தேனின் இருபடியான ஈத்தேன் என்பதற்குப் பதிலாக மீத்தேன் என்றே தவறாகப் புரிந்து கொண்டனர். இப்பிஒழை 1864 இல் காரல் சிகோர்லெமர் என்பவரால் சரிசெய்யப்பட்டது. இவ்வினைகளில் வழியாக உருவானது ஈத்தேன் என்பதை இவர் எடுத்துக்காட்டினார் [4].
கரிமச் சேர்மங்களுக்குப் பெயரிடும் ஐயுபிஏசி பெயரிடும் முறையில் இருந்து ஈத்தேன் என்ற பெயர் வருவிக்கப்பட்டுள்ளது. குடிக்கத்தக்க ஆல்ககால் (எத்தனால்) [5] என்ற பொருள் கொண்ட செருமன் மொழிச் சொல்லிலிருந்து ’ஈத்’ பெறப்பட்டு, அதனுடன் கார்பன் அணுக்களுக்கு இடையில் உள்ள ஒற்றைப் பிணைப்பைக் குறிப்பிடும் ஏன் என்ற சொல்லையும் சேர்த்து ஈத்தேன் என்ற சொல் உருவாக்கப்பட்டுள்ளது.
பண்புகள்
சாதாரண வெப்பநிலை மற்றும் அழுத்தத்தில் ஈத்தேன் நிறமற்று மணமற்று காணப்படுகிறது. இதனுடைய கொதிநிலை −88.5 °செல்சியசு வெப்பநிலை ஆகும். உருகுநிலை −182.8° செல்சியசு வெப்பநிலை ஆகும். திண்ம நிலை ஈத்தேன் பல்வேறு மாறுபாடுகளுடன் காணப்படுகிறது[6]. சாதாரண அழுத்தத்தில் குளிரூட்டும்போது முதலாவது மாறுபாடு நெகிழிப் படிகமாக கனசதுரத் திட்டத்தில் படிகமாகி தோன்றுகிறது. இவ்வடிவில் ஐதரசனின் இருப்பிடங்கள் நிலையானதல்ல. நீண்ட அச்சில் அவை சுதந்திரமாக சுழல்கின்றன. ஈத்தேன் தண்ணீரில் மிகச் சிறிதளவே கரைகின்றன.
வேதியியல்
ஈத்தேன் இரண்டு மெத்தில் குழுக்களால் ஆனது ஆகும். அதாவது, மெத்தில் குழுக்களின் இருபடியே ஈத்தேன் ஆகும். ஆய்வகத்தில் ஈத்தேன் கோல்ப் தொகுப்பு வினையினால் தயாரிக்கப்படுகிறது. இந்த நுட்ப வினையில் அசிட்டேட்டு உப்பின் நீரிய கரைசல் மின்னாற்பகுப்பு செய்யப்படுகிறது. எதிர்மின் முனையில் அசிட்டேட்டு ஆக்சிசனேற்றமடைந்து கார்பன் டை ஆக்சைடும் மெத்தில் இயங்குறுப்புகளும் உருவாகின்றன. மேலும் அதிகமான வினைத்திறன் கொண்ட இயங்குறுப்புகள் இணைந்து ஈத்தேன் உருவாகிறது.
மேற்கோள்கள்
- Faraday, Michael (1834). "Experimental researches in electricity: Seventh series". Philosophical Transactions 124: 77–122. doi:10.1098/rstl.1834.0008.
- Kolbe, Hermann; Frankland, Edward (1849). "On the products of the action of potassium on cyanide of ethyl". Journal of the Chemical Society 1: 60–74. doi:10.1039/QJ8490100060.
- Frankland, Edward (1850). "On the isolation of the organic radicals". Journal of the Chemical Society 2 (3): 263–296. doi:10.1039/QJ8500200263.
- Schorlemmer, Carl (1864). "Ueber die Identität des Aethylwasserstoffs und des Methyls". Annalen der Chemie und Pharmacie 132 (2): 234. doi:10.1002/jlac.18641320217.
- "the definition of ethyl".
- Van Nes, G.J.H.; Vos, A. (1978). "Single-crystal structures and electron density distributions of ethane, ethylene and acetylene. I. Single-crystal X-ray structure determinations of two modifications of ethane". Acta Crystallographica Section B 34 (6): 1947. doi:10.1107/S0567740878007037. http://www.rug.nl/research/portal/files/3440910/c3.pdf.
புற இணைப்புகள்
- International Chemical Safety Card 0266
- Market-Driven Evolution of Gas Processing Technologies for NGLs
- Staggered and eclipsed ethane
| ஆல்க்கேன்கள் | |||||||||||||||||||||||||||||||
|
மெத்தேன் |
| |
எத்தேன் |
| |
புரொப்பேன் |
| |
பியூட்டேன் |
| |
பென்ட்டேன் |
| |
எக்சேன் |
|||||||||||||||||||||
|
எப்டேன் |
| |
ஆக்டேன் |
| |
நோனேன் |
| |
டெக்கேன் |
| |
ஆண்டெக்கேன் |
| |
டோடெக்கேன் |
| ||||||||||||||||||||
