সোডিয়াম হাইড্রোক্সাইড
সোডিয়াম হাইড্রোক্সাইড একটি রাসায়নিক পদার্থ যা কস্টিক সোডা[2][3] নামে সমধিক পরিচিত। এটি একটি অজৈব যৌগ যার রাসায়নিক সংকেত NaOH। এটি সাদা কঠিন পদার্থ। বাজারে এটি পেলেট, ফ্লেইক, দানাদার এবং বিভিন্ন ঘনমাত্রার তরল দ্রবণ[6] আকারে লভ্য। সোডিয়াম হাইড্রোক্সাইড জলে দ্রবীভূত হয় এবং ৫০% সম্পৃক্ত দ্রবণ তৈরী করে[7]। সোডিয়াম হাইড্রোক্সাইড জল, ইথানল এবং মিথানলে দ্রবণীয়। এর ধর্ম ক্ষারকীয়। এই ক্ষার বাতাস থেকে ধীরে ধীরে আদ্র্তা এবং কার্বন ডাই অক্সাইড (CO2) শোষণ করে।
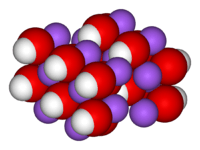 | |
 | |
| নামসমূহ | |
|---|---|
| পদ্ধতিগত আইইউপিএসি নাম
সোডিয়াম অক্সিডানাইড[1] | |
| অন্যান্য নাম | |
| শনাক্তকারী | |
সিএএস নম্বর |
|
ত্রিমাত্রিক মডেল (জেমল) |
|
| সিএইচইবিআই | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০১৩.৮০৫ |
| ইসি-নম্বর | 215-185-5 |
| ই নম্বর | E৫২৪ (অম্লতা নিয়ন্ত্রক, ...) |
| মেলিন রেফারেন্স | 68430 |
| কেইজিজি | |
| এমইএসএইচ | {{{value}}} |
পাবকেম CID |
|
| আরটিইসিএস নম্বর | WB4900000 |
| ইউএনআইআই | |
| ইউএন নম্বর | 1823 |
ইনকি
| |
এসএমআইএলইএস
| |
| বৈশিষ্ট্য | |
| NaOH | |
| আণবিক ভর | 39.9971 g mol−1 |
| বর্ণ | White, waxy, opaque crystals |
| গন্ধ | odorless |
| ঘনত্ব | 2.13 g/cm3 |
| গলনাঙ্ক | ৩১৮ °সে (৬০৪ °ফা; ৫৯১ K) |
| স্ফুটনাঙ্ক | ১,৩৮৮ °সে (২,৫৩০ °ফা; ১,৬৬১ K) |
পানিতে দ্রাব্যতা |
41.8 g/100 mL (0 °C) 111 g/100 mL (20 °C) 337 g/100 mL (100 °C) |
| দ্রাব্যতা | soluble in glycerol negligible in ammonia insoluble in ether |
| দ্রাব্যতা in methanol | 23.8 g/100 mL |
| দ্রাব্যতা in ethanol | <<13.9 g/100 mL |
| বাষ্প চাপ | <2.4 kPa (at 20 °C) |
| অম্লতা (pKa) | 13 |
| প্রতিসরাঙ্ক (nD) | 1.3576 |
| তাপ রসায়নবিদ্যা | |
| তাপ ধারকত্ব, C | 59.66 J/mol K |
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
64 J·mol−1·K−1[5] |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
−427 kJ·mol−1[5] |
গিবসের মুক্ত শক্তি (ΔfG˚) |
-380.7 kJ/mol |
| ঝুঁকি প্রবণতা | |
| জিএইচএস চিত্রলিপি |  |
ইইউ শ্রেণীবিভাগ (ডিএসডি) |
|
| আর-বাক্যাংশ | আর৩৫ |
| এস-বাক্যাংশ | (এস১/২), এস২৬, এস৩৭/৩৯, এস৪৫ |
| এনএফপিএ ৭০৪ | 
0
3
1 ALK |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ |
Sodium hydrosulfide |
অন্যান্য ক্যাটায়নসমূহ |
Caesium hydroxide Lithium hydroxide |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
বৈশিষ্ট্য
ভৌত ধর্ম
বিশুদ্ধ সোডিয়াম হাইড্রোক্সাইড সাদা রঙের কঠিন পদার্থ। এটি পেলেট, ফ্লেইক, এবং দানাদার অবস্থার পাশাপাশি তরল অবস্থাতে পাওয়া যায়। এটি পানিতে অতিমাত্রায় দ্রবণীয়। ইথানল এবং মিথানলে মৃদু দ্রবণীয়, ইথার এবং অপোলার দ্রাবকে অদ্রবণীয়। সালফিউরিক এসিডের জলযোজনের মত সোডিয়াম হাইড্রোক্সাইডকে পানিতে দ্রবীভূত করলে তাপোৎপাদী বিক্রিয়া সংগঠিত হয় এবং প্রচুর পরিমাণে তাপ উৎপন্ন হয়। উৎপন্ন দ্রবণটি বর্ণহীন এবং গন্ধহীন।
রাসায়নিক বৈশিষ্ট্য
অম্লের সাথে বিক্রিয়া
সোডিয়াম হাইড্রোক্সাইড (NaOH) প্রোটিক এসিডের সাথে বিক্রিয়া করে লবন ও পানি উৎপন্ন করে। উদাহরণস্বরূপ, সোডিয়াম হাইড্রোক্সাইড হাইড্রোক্লোরিক এসিড এর সাথে বিক্রিয়া করে সোডিয়াম ক্লোরাইড বা খাওয়ার লবণ গঠন করেঃ
সাধারণত, একটি সাধারণ আয়নিক সমীকরণের মাধ্যমে পুরো নিরপেক্ষ বিক্রিয়াটিকে নিম্নরূপে প্রকাশ করা যায়ঃ
শক্তিশালী এসিডের সাথে এই ধরনের বিক্রিয়ায় তাপ উৎপন্ন হয়। টাইট্রেশানের জন্য এই ধরনের এসিড বেজ বিক্রিয়া ব্যবহার করা হয়। হাইগ্রোসকপিক হওয়ার কারণে সোডিয়াম হাইড্রোক্সাইড (NaOH) কে প্রাথমিক স্ট্যান্ডার্ড হিসেবে ব্যবহার করা হয় না কারণ এটা বাতাস থেকে কার্বন ডাই অক্সাইড শোষণ করে।
এসিডিক অক্সাইডের সাথে বিক্রিয়া
সোডিয়াম হাইড্রোক্সাইড (NaOH) এসিড এনহাইড্রাইডস বা এসিড অক্সাইড যেমন সালফার ডাই অক্সাইডের সাথে বিক্রিয়া করে। এই ধরনের বিক্রিয়ার মাধ্যমে কয়লার দহনে উৎপন্ন ক্ষতিকর গ্যাসসমূহ বাতাসে মুক্ত হতে পারে না। উদাহরণস্বরূপঃ
- 2 NaOH + CO2→ Na2CO3 + H2O
ধাতু এবং অক্সাইডের সাথে বিক্রিয়া
অধঃক্ষেপ
সাবানিকরণ
এস্টার, এমাইডস এবং এলকাইল হ্যালাইডসের ক্ষার নির্ভর হাইড্রোলাইসিসে সোডিয়াম হাইড্রোক্সাইড ব্যবহার করা যায়। জৈব যৌগে সোডিয়াম হাইড্রোক্সাইডের কম দ্রবীভূত হওয়ার কারণে দ্রবনীয় পটাশিয়াম হাইড্রোক্সাইড ব্যবহার করা হয়।
উৎপাদন
বাংলাদেশে সোডিয়াম হাইড্রোক্সাইড উৎপাদন
ব্যবহার
সোডিয়াম হাইড্রোক্সাইড বিবিধ শিল্প কলকারখানায় ব্যবহৃত হয়। বিশেষ করে পাল্প এবং কাগজ, টেক্সটাইল, সাবান এবং ডিটারজেন্টস, পানীয় জল, নর্দমা পরিষ্কার ইত্যাদিতে সোডিয়াম হাইড্রোক্সাইডের বহুল ব্যবহার হয়। ২০০৪ খ্রিষ্টাব্দে সারা বিশ্বে সোডিয়াম হাইড্রোক্সাইডের চাহিদা ছিলো ৫১ মিলিয়ন টন। বছর শেষে সোডিয়াম হাইড্রোক্সাইড উৎপাদন হয়েছিল মোট ৬০ মিলিয়ন টন।
নিরাপত্তা
তথ্যসূত্র
- http://en.chembase.cn/substance-371462.html
- "Material Safety Datasheet" (PDF)।
- "Material Safety Datasheet 2" (PDF)। ৩ আগস্ট ২০১২ তারিখে মূল (PDF) থেকে আর্কাইভ করা। সংগ্রহের তারিখ ১৯ জুলাই ২০১৪।
- Zumdahl, Steven S. (২০০৯)। Chemical Principles 6th Ed.। Houghton Mifflin Company। পৃষ্ঠা A23। আইএসবিএন 0-618-94690-X।
- http://www.sigmaaldrich.com/analytical-chromatography/analytical-products.html?TablePage=103242111
- http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=14798&loc=ec_rcs#x27
আরো দেখুন
- সোডিয়াম
- সাধারন রাসায়নিক
- সোডিয়াম ক্লোরাইড
- ব্রাইন
বইয়ে পড়ুন
- ইউরো ক্লোর - কিভাবে ক্লোরিন তৈরী হয় Chlorine Online
- Greenwood, N. N.; Earnshaw, A. (১৯৯৭)। Chemistry of the Elements (2nd সংস্করণ)। Butterworth-Heinemann। আইএসবিএন 0080379419।
- Heaton, A. (১৯৯৬) An Introduction to Industrial Chemistry, 3rd edition, New York:Blackie. আইএসবিএন ০-৭৫১৪-০২৭২-৯.
বহিঃসংযোগ
| উইকিমিডিয়া কমন্সে সোডিয়াম হাইড্রোক্সাইড সংক্রান্ত মিডিয়া রয়েছে। |
| উইকিঅভিধানে সোডিয়াম হাইড্রোক্সাইড শব্দটি খুঁজুন। |
| উইকিমিডিয়া কমন্সে সোডিয়াম হাইড্রোক্সাইড সংক্রান্ত মিডিয়া রয়েছে। |
- আন্তঃর্জাতিক রাসায়নিক নিরাপত্তা কার্ড ০৩৬০
- NIOSH Pocket Guide to Chemical Hazards
- CDC - Sodium Hydroxide - NIOSH Workplace Safety and Health Topic
- European Union Risk Assessment Report
- ব্রাইন তড়িৎ বিশ্লেষণ থেকে উৎপাদন
- সোডিয়াম হাইড্রোক্সাইড সেফটি ডাটা শিট(SDS)
- Titration of acids with sodium hydroxide; freeware for data analysis, simulation of curves and pH calculation
- Caustic soda production in continuous causticising plant by lime soda process