পটাসিয়াম হাইড্রোক্সাইড
পটাসিয়াম হাইড্রোক্সাইড একটি অজৈব যৌগ, যার রাসায়নিক সংকেত KOH । এটি সাধারণত কষ্টিক পটাশ নামে পরিচিত ।
 | |
 | |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
Potassium hydroxide | |
| অন্যান্য নাম
কষ্টিক পটাশ , Potash lye, পটাসিয়া, পটাসিয়াম হাইড্রেট | |
| শনাক্তকারী | |
সিএএস নম্বর |
|
ত্রিমাত্রিক মডেল (জেমল) |
|
| সিএইচইবিআই | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০১৩.৮০২ |
| ইসি-নম্বর | 215-181-3 |
| ই নম্বর | E৫২৫ (অম্লতা নিয়ন্ত্রক, ...) |
পাবকেম CID |
|
| আরটিইসিএস নম্বর | TT2100000 |
| ইউএনআইআই | |
| ইউএন নম্বর | 1813 |
ইনকি
| |
এসএমআইএলইএস
| |
| বৈশিষ্ট্য | |
| HKO | |
| আণবিক ভর | ৫৬.১১ g·mol−১ |
| বর্ণ | সাদা কঠিন, গলনশীল |
| গন্ধ | গন্ধহীন |
| ঘনত্ব | ২.০৪৪ g/cm3 (20 °C)[1] 2.12 g/cm3 (25 °C)[2] |
| গলনাঙ্ক | ৪০৬ °সে (৭৬৩ °ফা; ৬৭৯ K) |
| স্ফুটনাঙ্ক | ১,৩২৭ °সে (২,৪২১ °ফা; ১,৬০০ K) |
পানিতে দ্রাব্যতা |
85 g/100 g (-23.2 °C) 97 g/100 mL (0 °C) 121 g/100 mL (25 °C) 138.3 g/100 mL (50 °C) 162.9 g/100 mL (100 °C)[1][3] |
| দ্রাব্যতা | soluble in alcohol, glycerol insoluble in ether, liquid ammonia |
| দ্রাব্যতা in methanol | 55 g/100 g (28 °C)[2] |
| অম্লতা (pKa) | 13.5 (0.1 M) |
| প্রতিসরাঙ্ক (nD) | 1.409 (20 °C) |
| গঠন | |
| স্ফটিক গঠন | rhombohedral |
| তাপ রসায়নবিদ্যা | |
| তাপ ধারকত্ব, C | 65.87 J/mol•K[2] |
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
79.32 J/mol•K[2][4] |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
-425.8 kJ/mol[2][4] |
গিবসের মুক্ত শক্তি (ΔfG˚) |
-380.2 kJ/mol[2] |
| ঝুঁকি প্রবণতা | |
| জিএইচএস চিত্রলিপি |   |
| জিএইচএস সাংকেতিক শব্দ | Danger |
| জিএইচএস বিপত্তি বিবৃতি | H302, H314[5] |
| জিএইচএস সতর্কতামূলক বিবৃতি | P280, P305+351+338, P310[5] |
ইইউ শ্রেণীবিভাগ (ডিএসডি) |
|
| আর-বাক্যাংশ | আর২২, আর৩৫ |
| এস-বাক্যাংশ | (এস১/২), এস২৬, এস৩৬/৩৭/৩৯, এস৪৫ |
| এনএফপিএ ৭০৪ | 
0
3
1 |
| ফ্ল্যাশ পয়েন্ট | Non-flammable |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ) |
273 mg/kg (oral, rat)[6] |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ |
পটিাসিয়াম হাইড্রোসালফাইড পটিাসিয়াম অ্যামাইড |
অন্যান্য ক্যাটায়নসমূহ |
লিথিয়াম হাইড্রোক্সাইড সোডিয়াম হাইড্রোক্সাইড রুবিডিয়াম হাইড্রোক্সাইড সিজিয়াম হাইড্রোক্সাইড |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
এই বর্ণহীন কঠিন পদার্থ সোডিয়াম হাইড্রোক্সাইড এর মতই একটি তীব্র ক্ষার । প্রতি বছর NaOH এর চেয়ে প্রায় ১০০ গুণ বেশি KOH উৎপন্ন করা হয় ।[7]
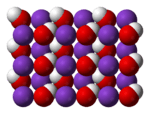
বৈশিষ্ট্য এবং গঠন
অবিশুদ্ধ পটাসিয়াম এর সাথে সোডিয়াম হাইড্রোক্সাইড এর বিক্রিয়ায় বিশুদ্ধ পটাসিয়াম হাইড্রোক্সাইড পাওয়া সম্ভব । এটি সাধারণত ষদচ্ছ ক্ষুদ্র বড়ি আকারে বিক্রয় করা হয়, যা সহজেই আঠাল হয়ে যায়, কারণ এটি জলগ্রাহী ।
গঠন
দ্রাব্যতা এবং শুষ্কতা
তথ্যসূত্র
- Lide, D. R., সম্পাদক (২০০৫)। CRC Handbook of Chemistry and Physics (86th সংস্করণ)। Boca Raton (FL): CRC Press। পৃষ্ঠা 4-80। আইএসবিএন 0-8493-0486-5।
- http://chemister.ru/Database/properties-en.php?dbid=1&id=325
- Seidell, Atherton; Linke, William F. (১৯৫২)। [Google Books Solubilities of Inorganic and Organic Compounds]
|ইউআরএল=এর মান পরীক্ষা করুন (সাহায্য)। Van Nostrand। সংগ্রহের তারিখ ২০১৪-০৫-২৯। - Zumdahl, Steven S. (২০০৯)। Chemical Principles 6th Ed.। Houghton Mifflin Company। পৃষ্ঠা A22। আইএসবিএন 0-618-94690-X।
- Sigma-Aldrich Co., Potassium hydroxide. Retrieved on 2014-05-18.
- http://chem.sis.nlm.nih.gov/chemidplus/rn/1310-58-3
- H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim.
This article is issued from
Wikipedia.
The text is licensed under Creative
Commons - Attribution - Sharealike.
Additional terms may apply for the media files.