2-பியூட்டனால்
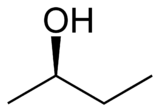
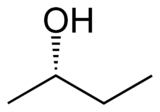
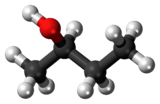
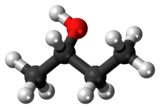
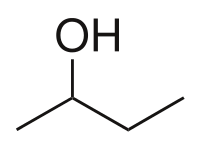
2-பியூட்டனால் (2-Butanol) என்பது CH3CH(OH)CH2CH3 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கரிம வேதியியல் சேர்மமாகும். இதை ஈரிணைய பியூட்டனால் என்ற பெயராலும் அழைக்கலாம். நிறமற்ற நீர்மமான இந்த ஈரிணைய ஆல்ககால் எளிதில் தீப்பிடித்து எரியும். தண்ணீரில் மூன்று பகுதிகள் கரையும். கரிமக் கரைப்பான்களில் நன்றாக கலக்கும். பேரளவில் தயாரிக்கப்படும் 2-பியூட்டனால் தொழிற்சாலை கரைப்பான மெத்தில் எத்தில் கீட்டோன் தயாரிப்பதற்கு பயன்படும் ஒரு முன்னோடிச் சேர்மமாகும். 2-பியூட்டனால் ஒரு படியா மூலக்கூறு எனப்படுவதால் வலஞ்சுழி-(−)-2-பியூட்டனால் அல்லது இடஞ்சுழி-(+)-2- என்ற முப்பரிமாண மாற்றியங்கள் இரண்டில் ஒன்று உருவாகும். பொதுவாக இரண்டு முப்பரிமாண மாற்றியங்களில் 1:1 என்ற விகிதத்திலான சமதிருப்பக் கலவையாகத் தோன்றுகிறது.
 |  |
 |  |
 | |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
பியூட்டேன்-2-ஆல்[1] | |
| வேறு பெயர்கள் | |
| இனங்காட்டிகள் | |
| 78-92-2 14898-79-4 (R) 4221-99-2 (S) | |
Beilstein Reference |
773649 1718764 (R) |
| ChEBI | CHEBI:35687 |
| ChEMBL | ChEMBL45462 |
| ChemSpider | 6320 76392 (R) 392543 (S) |
| DrugBank | DB02606 |
| EC number | 201-158-5 |
Gmelin Reference |
1686 396584 (R) |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| ம.பா.த | 2-பியூட்டனால் |
| பப்கெம் | 6568 84682 (R) 444683 (S) |
| வே.ந.வி.ப எண் | EO1750000 |
SMILES
| |
| UN number | 1120 |
| பண்புகள் | |
| C4H10O | |
| வாய்ப்பாட்டு எடை | 74.12 g·mol−1 |
| அடர்த்தி | 0.808 கிராம் செ.மீ−3 |
| உருகுநிலை | |
| கொதிநிலை | 98 to 100 °C; 208 to 212 °F; 371 to 373 K |
| 290 கி/லிட்டர்[3] | |
| மட. P | 0.683 |
| ஆவியமுக்கம் | 1.67 கிலோபாசுக்கல் (20 °செல்சியசில்) |
| காடித்தன்மை எண் (pKa) | 17.6 [4] |
காந்த ஏற்புத்திறன் (χ) |
−5.7683×10−5 செ.மீ3 மோல்−1 |
| ஒளிவிலகல் சுட்டெண் (nD) | 1.3978 (20 °செல்சியசில்) |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
−343.3 to −342.1 kJ மோல்−1 |
| Std enthalpy of combustion ΔcH |
−2.6611 to −2.6601 MJ மோல்−1 |
| நியம மோலார் எந்திரோப்பி S |
213.1 J கெல்வின்−1 மோல்−1 |
| வெப்பக் கொண்மை, C | 197.1 J கெல்வின்−1 மோல்−1 |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | inchem.org |
| GHS pictograms |   |
| GHS signal word | எச்சரிக்கை |
| H226, H319, H335, H336 | |
| P261, P305+351+338 | |
| தீப்பற்றும் வெப்பநிலை | 22 to 27 °C (72 to 81 °F; 295 to 300 K) |
Autoignition temperature |
405 °C (761 °F; 678 K) |
| வெடிபொருள் வரம்புகள் | 1.7–9.8% |
| Lethal dose or concentration (LD, LC): | |
LCLo (Lowest published) |
மில்லியனுக்கு 16,000 பகுதிகள் (எலி, 4 hr) மில்லியனுக்கு 10,670 பகுதிகள் (சுண்டெலி, 3.75 hr) மில்லியனுக்கு 16,000 பகுதிகள் (சுண்டெலி, 2.67 hr)[5] |
| அமெரிக்க சுகாதார ஏற்பு வரம்புகள்: | |
அனுமதிக்கத்தக்க வரம்பு |
டி டபிள்யூ ஏ மில்லியனுக்கு 150 பகுதிகள் (450 மி.கி/மீ3)[5] |
பரிந்துரைக்கப்பட்ட வரம்பு |
TWA மில்லியனுக்கு 100 பகுதிகள் (305 mg/m3) எசு.டி மில்லியனுக்கு 150 பகுதிகள் (455 மி.கி/மீ3)[5] |
உடனடி அபாயம் |
மில்லியனுக்கு 2000 பகுதிகள்[5] |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| | |
| Infobox references | |
தயாரிப்பும் பயன்களும்
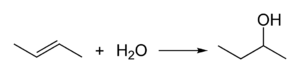
1-பியூட்டீன் அல்லது 2-பியூட்டீன் சேர்மம் நீரேற்றம் செய்யப்பட்டு தொழில்துறை ரீதியாக 2-பியூட்டனால் தயாரிக்கப்படுகிறது :
கந்தக அமிலம் இவ்வினை மாற்றத்திற்கு வினையூக்கியாகப் பயன்படுத்தப்படுகிறது..[6] ஆய்வகத்தில் இது கிரிக்னார்டு வினை வழியாக தயாரிக்கப்படுகிறது. உலர்ந்த டை எத்தில் ஈதர் அல்லது டெட்ரா ஐதரோபியூரான் உடன் அசிடால்டிகைடும் எத்தில்மக்னீசியம் புரோமைடும் சேர்ந்து வினைபுரிவதால் 2-பியூட்டனால் உருவாகிறது. சிறிதளவு 2- பியூட்டனால் ஒரு கரைப்பானாகப் பயன்படுத்தப்பட்டாலும், முக்கியமாக பியூட்டானோன் எனப்படும் மெத்தில் எத்தில் கீட்டோன் சேர்மமாகவே மாற்றப்படுகிறது, இது ஒரு முக்கியமான தொழில்துறை கரைப்பான் ஆகும். பல உள்நாட்டு துப்புரவு முகவர்கள் மற்றும் சாய நீக்கிகளில் இது காணப்படுகிறது. 2-பியூட்டனாலின் ஆவியாகும் எசுத்தர்கள் இனிமையான நறுமணங்களைக் கொண்டிருக்கின்றன, மேலும் அவை சிறிய அளவில் வாசனை திரவியங்களாகவோ அல்லது செயற்கை சுவைகளிலோ பயன்படுத்தப்படுகின்றன[6]
கரைதிறன்
2-பியூட்டனாலின் கரைதிறன் பெரும்பாலான ஆதார மூலங்களில் தவறானது[3]. மெர்க் இன்டெக்சு சி.ஆர்.சி வேதியியல் புத்தக கையேடு மற்றும் இயற்பியல் மற்றும் லாங்கேவின் வேதியியல் கையேடு போன்ற மிகவும் பிரபலமான மேற்கோள்களும் இதில் உள்ளடங்கி உள்ளன. வேதியியல் பாதுகாப்பு குறித்த பன்னாட்டு திட்டம் கூட தவறான கரைதிறனை பட்டியலிடுகிறது. இந்த பரவலான பிழை பீல்சுடீனின் கரிம வேதியியல் கையேடு நூலின் காரணமாக உருவானது. இந்த நூலில் 100 கிராம் நீரில் 2-பியூட்டனாலின் கரைதிறன் 12.5 கிராம் என்று தவறாக கரைதிறனை மேற்கோளிடுகிறது. தொடர்ந்து பல ஆதார மூலங்கள் இந்த கரைதிறனைப் பயன்படுத்தின, இது தொழில்துறை உலகில் பரவலாகப் பயன்படுத்தப்பட்டு ஒரு பிழையாக மாறியுள்ளது. சரியான கரைதிறன் 20 பாகை செல்சியசு வெப்பநிலையில் 35.0 கிராம் / 100 கிராம், 25 பாகை செல்சியசு வெப்பநிலையில் 29 கிராம் / 100 கிராம், மற்றும் 30 பாகை செல்சியசு வெப்பநிலையில் 22 கிராம் / 100 கிராம் என்று முதன்முதலில் 1886 ஆம் ஆண்டில் அலெக்சீவால் வெளியிடப்பட்டது[3].
பாதுகாப்பு
மற்ற பியூட்டனால்களைப் போலவே 2-பியூட்டனாலும் குறைந்த கடுமையான நச்சுத்தன்மையைக் கொண்டுள்ளது. இதன் உயிர்க்கொல்லும் அளவு எலிகளுக்கு வாய்வழியாக கொடுக்கும் போது கிலோகிராமுக்கு 4400 மில்லி கிராம் ஆகும்[6]. 2-பியூட்டனால் சேர்மத்தை வழக்கமாக காய்ச்சி வடிகட்டும் போது பல வெடிப்பு நிகழ்வுகள் அறியப்பட்டுள்ளனref>Doyle, R. R. (1986). "2-Butanol safety warning". Journal of Chemical Education 63 (2): 186. doi:10.1021/ed063p186.2., and references cited therein.</ref>.. தூய ஆல்ககால்களின் கொதிநிலையை விட அதிக கொதிநிலையுடன் பெராக்சைடு உருவாக்கம் இருப்பதால் இவ்வெடி விபத்துகள் நிகழ்கின்றன. ஆல்ககால்கள், ஈத்தர்களைப் போலன்றி, பெராக்சைடு அசுத்தங்களை உருவாக்கும் திறன் கொண்டதாக பரவலாக அறியப்படாததால் ஆபத்து கவனிக்கப்படாமல் போகக்கூடும்.
மேற்கோள்கள்
- "2-butanol - Compound Summary". PubChem Compound. USA: National Center for Biotechnology Information (26 March 2005). பார்த்த நாள் 12 October 2011.
- "Alcohols Rule C-201.1". Nomenclature of Organic Chemistry (The IUPAC 'Blue Book'), Sections A, B, C, D, E, F, and H. Oxford: Pergamon Press. 1979. "Designations such as isopropanol, sec-butanol, and tert-butanol are incorrect because there are no hydrocarbons isopropane, sec-butane, and tert-butane to which the suffix "-ol" can be added; such names should be abandoned. Isopropyl alcohol, sec-butyl alcohol, and tert-butyl alcohol are, however, permissible (see Rule C-201.3) because the radicals isopropyl, sec-butyl, and tert-butyl do exist."
- Alger, Donald B. (November 1991). "The water solubility of 2-butanol: A widespread error". Journal of Chemical Education 68 (11): 939. doi:10.1021/ed068p939.1.
- Serjeant, E.P., Dempsey B.; Ionisation Constants of Organic Acids in Aqueous Solution. International Union of Pure and Applied Chemistry (IUPAC). IUPAC Chemical Data Series No. 23, 1979. New York, New York: Pergamon Press, Inc., p. 989
- "NIOSH Pocket Guide to Chemical Hazards #0077". National Institute for Occupational Safety and Health (NIOSH).
- Hahn, Heinz-Dieter; Dämbkes, Georg; Rupprich, Norbert (2005), "Butanols", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH.
புற இணைப்புகள்
- International Chemical Safety Card 0112
- "NIOSH Pocket Guide to Chemical Hazards #0077". National Institute for Occupational Safety and Health (NIOSH).