ইথিন
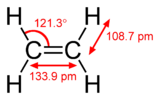
ইথিন বা ইথিলিন একটি এলিফ্যাটিক হাইড্রোকার্বন, এর সমগোত্রীয় শ্রেণীর অণুতে কার্বন=কার্বন দ্বিবন্ধন (C=C) বিদ্যমান। ইথিন সাধারণভাবে এলকিন বা অলেফিনস নামে পরিচিত। লাতিন অলেফিনস মানে তৈল উৎপাদনকারী। এই যৌগগুলো ক্লোরিনের সাথে বিক্রিয়া করে ডাইক্লোরাইড গঠন করে যা তৈলজাতীয় যৌগ।
- CH2= CH2 + Cl2 = CH2Cl-CH2Cl
 | |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
ইথিন | |
| অন্যান্য নাম
ইথিলিন | |
| শনাক্তকারী | |
সিএএস নম্বর |
|
ত্রিমাত্রিক মডেল (জেমল) |
|
| সিএইচইবিআই | |
| সিএইচইএমবিএল | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.৭৪২ |
| কেইজিজি | |
পাবকেম CID |
|
| ইউএনআইআই | |
ইনকি
| |
এসএমআইএলইএস
| |
| বৈশিষ্ট্য | |
| C 2H 4 | |
| আণবিক ভর | 28.05 g/mol |
| বর্ণ | colorless gas |
| ঘনত্ব | 1.178 kg/m3 at 15 °C, gas[1] |
| গলনাঙ্ক | −169.2 °C (104.0 K, -272.6 °F) |
| স্ফুটনাঙ্ক | −103.7 °C (169.5 K, -154.7 °F) |
পানিতে দ্রাব্যতা |
3.5 mg/100 mL (17 °C) ; 2.9 mg/L[2] |
| দ্রাব্যতা in ইথানল | 4.22 mg/L[2] |
| দ্রাব্যতা in ডাই ইথাইল ইথার | উত্তম[2] |
| অম্লতা (pKa) | 44 |
| গঠন | |
| আণবিক আকৃতি | D2h |
| ডায়াপল মুহূর্ত | zero |
| তাপ রসায়নবিদ্যা | |
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
219.32 J·K−1·mol−1 |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
+52.47 kJ/mol |
| ঝুঁকি প্রবণতা | |
ইইউ শ্রেণীবিভাগ (ডিএসডি) |
Extremely flammable (F+) |
| এনএফপিএ ৭০৪ | 
4
1
2 |
| ফ্ল্যাশ পয়েন্ট | −১৩৬ °সে (−২১৩ °ফা; ১৩৭ K) |
| সম্পর্কিত যৌগ | |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
এটি একটি মুক্ত শিকল এলকিন।
সংকেত
- ইথিনের রাসায়নিক সংকেতঃ C2H4
ইথিনের রাসায়নিক সংকেতঃ CH2=CH2
উৎস
প্রকৃতিতে প্রাপ্ত
ইথিন দুই পদ্ধতিতে উৎপাদন করা যায়। ভাঙন বা ক্রাকিং পদ্ধতিতে পেট্রোলিয়াম থেকে প্রাপ্ত হাইড্রোকার্বন থেকে এটি আহরণ করা হয়। আমেরিকায় প্রাকৃতিক গ্যাস এবং ইউরোপে অপরিশোধিত তেলের ন্যাপথা অংশ থেকে ইথিন পাওয়া যায়। করে।[3]
উচ্চ তাপমাত্রা ও চাপে ইথেনকে ভাঙলে ইথিন পাওয়া যায়। সেই সাথে কিছু এলকেনও উৎপন্ন হয়। ইথেন ---> ইথিন + এলকেন
পরীক্ষাগারে প্রস্তুতি
পরীক্ষাগারে অধিক পরিমাণ গাঢ় সালফিউরিক এসিডের সাথে ইথানলকে উত্তপ্ত করলে ইথিন উৎপন্ন হয়।
CH2-OH + H2SO4 = R=CH2 + (H2O + H2SO4)
শিল্পোৎপাদন পদ্ধতি
শিল্প কারখানায় ইথিন উৎপাদনে বেশ কয়েকটি পদ্ধতি অনুসরণ করা হয়।
এলকোহল থেকে
ইথানলকে উচ্চ তাপমাত্রায় এলুমিনিয়াম অক্সাইডের উপর দিয়ে প্রবাহিত করলে প্রচুর পরিমাণে ইথিন উৎপন্ন হয়। এক্ষেত্রে এলুমিনা (AL2O3) নিরুদক হিসেবে কাজ করে।
ইথাইন থেকে
লেড এবং বেরিয়াম সালফেট এর উপস্থিতিতে ইথাইনএর সাথে হাইড্রোজেন যুক্ত হয়ে ইথিন উৎপন্ন করে।
বৈশিষ্ট্য
স্বাভাবিক তাপমাত্রায় গ্যাসীয়/তরল। ইথিন ইথেনের ন্যায় অপোলার জৈব দ্রাবকে দ্রবনীয় কিন্তু পোলার দ্রাবক যেমন পানিতে অদ্রবনীয়। ইথিনের সাথে নিকেল প্রভাবকের উপস্থিতিতে হাইড্রোজেন অণু যুক্ত হয়ে ইথেন তৈরী করে।[4]
ব্যবহার
১- কাচা ফল পাকাতে ২- মিডেহদু রান্না করতে
তথ্যসূত্র
- Record of Ethylene in the GESTIS Substance Database from the IFA, accessed on 25 October 2007
- Нейланд О. Я. Органическая химия: Учебник для хим. спец. вузов.— Москва: Высшая школа, 1990.— с. 128
- উচ্চ মাধ্যমিক রসায়ন, দ্বিতীয় পত্র, হাজারী এবং নাগ।
- উচ্চ মাধ্যমিক রসায়ন, দ্বিতীয় পত্র, ড. মোঃ রবিউল ইসলাম, ড. গাজী মোঃ আহসানুল কবীর, ড. মোঃ মনিমুল হক।