மக்னீசியம் இரும்பு எக்சா ஐதரைடு
மக்னீசியம் இரும்பு எக்சா ஐதரைடு (Magnesium iron hexahydride) என்பது Mg2FeH6 என்ற மூலக்கூற்று வாய்ப்பாட்டால் விவரிக்கப்படும் ஒரு கனிம வேதியியல் சேர்மமாகும். பச்சை நிறத்தில் டயாகாந்தப்பண்பு கொண்ட திண்மமான இச்சேர்மம் உலர் காற்றில் நிலைப்புத்தன்மையுடன் காணப்படுகிறது. உயர் அழுத்தத்தில் உள்ள ஐதரசனில் தூளாகக் கலக்கப்பட்ட மக்னீசியம் மற்றும் இரும்பு தனிமங்களின் கலவையை சூடுபடுத்தி மக்னீசியம் இரும்பு எக்சா ஐதரைடு தயாரிக்கப்படுகிறது :[1]
- 2 Mg + Fe + 3 H2 → Mg2FeH6.
 | |
| பெயர்கள் | |
|---|---|
| வேறு பெயர்கள்
டைமக்னீசியம் இரும்பு எக்சா ஐதரைடு | |
| பண்புகள் | |
| FeH6Mg2 | |
| வாய்ப்பாட்டு எடை | 110.50 g·mol−1 |
| தோற்றம் | பச்சை நிறத் திண்மம் |
| அடர்த்தி | 2.74 கி/செ.மீ3 |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
| Infobox references | |
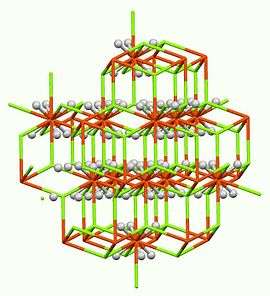
கட்டமைப்பு
K2PtCl6 சேர்மத்துடன் இச்சேர்மம் சமவுருவக் கட்டமைப்பைக் கொண்டுள்ளது. அதாவது, அவற்றின் இணைப்பிகளும் கட்டமைப்புகளும் ஒரேமாதிரியாக இருக்கின்றன. [FeH6]4− மையம் 1.56 Å என்ற அளவில் Fe-H பிணைப்பு இடைவெளி கொண்ட எண்முக மூலக்கூற்று வடிவத்தை ஏற்றுக்கொள்கிறது. Mg2 + மையங்கள் 2.38 Å என்ற தொலைவை Mg-H பிணைப்பு இடைவெளியாகக் கொண்டு எண் கோணத்தின் முகப்புகளுடன் பிணைக்கப்பட்டுள்ளன. மேலும், [RuH6]4−, [OsH6]4− மற்றும் [PtH6]2− உள்ளிட்ட எதிர்மின் அயனிகளைக் கொண்ட தொடர்புடைய பல சேர்மங்கள் அறியப்படுகின்றன [2].
கரையும் வழிப்பெறுதிகள்
சாதாரணக் கரைப்பான்களில் Mg2FeH6 கரையாது என்றபோதிலும் தொடர்புடைய சில சேர்மங்கள் கரைகின்றன. உதாரணமாக தொடர்புடைய Mg4Br4(THF)4FeH6 .என்ற உப்பு தொடர்புடைய ஆல்காக்சைடுகள் போல கரைகிறது. ஐதரைடு ஈந்தணைவிகள் சயனைடுகளைக் காட்டிலும் பலவீனமான படிகப் புலத்தை வெளிப்படுத்துகின்றன என்பதை அச்சேர்மங்களைப் பற்றிய கணக்கீடுகள் தெரிவிக்கின்றன [3].
மேற்கோள்கள்
- J. J. Didisheim, P. Zolliker, K. Yvon, P. Fischer, J. Schefer, M. Gubelmann, A. F. Williams "Dimagnesium iron(II) hydride, Mg2FeH6, containing octahedral FeH64− anions" Inorganic Chemistry 1984, vol. 23, pp 1953–1957. எஆசு:10.1021/ic00181a032.
- Robert Bau, Mary H. Drabnis "Structures of transition metal hydrides determined by neutron diffraction" Inorganica Chimica Acta 1997, vol. 259, 27ff.எஆசு:10.1016/S0020-1693(97)89125-6
- R.B. King "Structure and bonding in homoleptic transition metal hydride anions" Coordination Chemistry Reviews, 2000, vol. 200–202, p. 813–829. எஆசு:10.1016/S0010-8545(00)00263-0