கார்பாக்சிலிக் அமிலம்
கார்பாக்சிலிக் அமிலம் (carboxylic acid) என்பது தன்னுடைய கட்டமைப்பில் குறைந்தது ஒரு கார்பாக்சில் குழுவையாவது (C(=O)OH) [1] கொண்டுள்ள கரிமச்சேர்மம் கார்பாக்சிலிக் அமிலம் எனப்படுகிறது. இதனுடைய அமைப்பு வாய்ப்பாடு R–COOH, ஆகும். இவ்வாய்ப்பாட்டிலுள்ள R என்பது ஆல்க்கைல் அல்லது ஓர் அரைல் மூலக்கூறைக் குறிக்கிறது. கார்பாக்சிலிக் அமிலங்கள் பரவலாகத் தோன்றுகின்றன. புரதங்களை உருவாக்கும் அமினோ அமிலங்கள், வினீகரின் ஒரு பகுதியாகவும் வளர்சிதை மாற்றத்தில் உருவாகக் கூடியதுமான அசிட்டிக் அமிலம் உள்ளிட்டவையும் கார்பாக்சிலிக் அமிலங்களே ஆகும்.
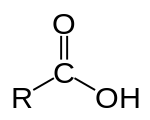
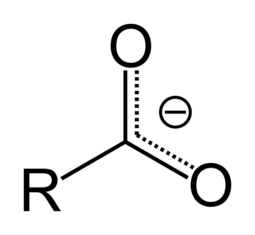
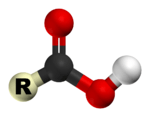
கார்பாக்சிலிக் அமிலத்தின் உப்புகளும் எசுத்தர்களும் கார்பாக்சிலேட்டுகள் எனப்படுகின்றன. ஒரு கார்பாக்சில் குழு புரோட்டான் நீக்கம் செய்யப்பட்டால் அதனுடைய இணை காரம் ஒரு கார்பாக்சிலேட்டு எதிர்மின் அயனியை உருவாக்குகிறது. கார்பாக்சிலேட்டு அயனிகள் ஒத்திசைவால் உறுதிப்படுத்தப்பட்டவை ஆகும். இந்த அதிகரிக்கப்பட்ட நிலைப்புத்தன்மை கார்பாக்சிலிக் அமிலங்களை ஆல்ககால்களைக் காட்டிலும் அதிக அமிலத்தன்மை கொண்டவையாக ஆக்குகின்றன.
உதாரணங்களும் பெயரியலும்
கார்பாக்சிலிக் அமிலங்கள் பொதுவாக அவற்றின் எளிய திட்டம் சாரா பெயர்களைப் பயன்படுத்தி அடையாளம் காணப்படுகின்றன. வழக்கமாக அவற்றின் பின்னொட்டு இக் அமிலம் என்று முடிவு பெறுவனவாக இருக்கும். இவற்ருக்கு ஐயுபிஏசி முறையில் பரிந்துரைக்கப்பட்ட பெயர்களும் உள்ளன.இம்முறையில் கார்பாக்சிலிக் அமிலங்கல் ஆயிக் அமிலம் என்ற பின்னொட்டைக் கொண்டு முடிவனவாக இருக்கின்றன [2].
உதாரணமாக எளிய முறையில் பியூட்டைரிக் அமிலம் (C3H7CO2H) என்று அழைக்கப்படும் கார்பாக்சிலிக் அமிலம் ஐயுபிஏசி முறையில் பியூட்டனாயிக் அமிலம் என்று அழைக்கப்படுகிறது.
ஒரு கார்பாக்சிலிக் அமிலத்தைக் கொண்டிருக்கும் அணைவுச் சேர்மங்களுக்குப் பெயரிடும் போது வேறு பதிலீடுகள் இருந்தாலும் தாய்சங்கிலியில் கார்பாக்சிலிக் அமிலம் இணைந்துள்ள இடத்திற்கு முதலாவது எண் கொடுக்கப்படுகிறது. உதாரணமாக கார்பாக்சி அல்லது கார்பாக்சிலிக் அமிலம் என்று பெயரிடுவதற்குப் பதிலாக 3-குளோரோபுரோப்பியானிக் அமிலம் எனப்படுகிறது. வேறொரு தாய்கட்டமைப்புடன் கார்பாக்சில் குழு இணைந்திருந்தால் அதை 2-கார்பாக்சிபியூரான் என்று கார்பாக்சி குழு முன்னிலைப்படுத்தப்பட்டு பெயரிடப்படுகிறது.
கார்பாக்சிலிக் அமிலத்தின் கார்பாக்சிலேட்டு எதிர்மின் அயனி (R–COO−) பொதுவாக ஏட்டு என்ற பின்னொட்டுடன் சேர்த்து பெயரிடப்படுகிறது. மேலும் பொது வழக்கில் இணை அமிலத்திற்கு இக் என்ற பின்னொட்டும் இணை காரத்திற்கு ஏட்டு என்ற பின்னொட்டும் சேர்த்து அழைக்கப்படுகிறது. உதாரணமாக அசிட்டிக் அமிலத்தின் இணை காரம் அசிட்டேட்டு எனப் பெயரிடப்படுகிறது.
| Carbon அணுக்கள் |
பொதுப் பெயர் | ஐயுபிஏசி பெயர் | வாய்ப்பாடு | பொது அமைவிடம் அல்லது பயன் |
|---|---|---|---|---|
| 1 | கார்பானிக் அமிலம் | கார்பனாயிக் அமிலம் | OHCOOH | இரத்தம் மற்றும் திசுக்கள் |
| 1 | ஃபார்மிக் அமிலம் | மெத்தனாயிக் அமிலம் | HCOOH | பூச்சிகளின் கொடுக்கு |
| 2 | அசிட்டிக் அமிலம் | எத்தனாயிக் அமிலம் | CH3COOH | வினீகர் |
| 3 | புரோப்பியோனிக் அமிலம் | புரோப்பனாயிக் அமிலம் | CH3CH2COOH | உடல் நெடி |
| 4 | பியூட்டைரிக் அமிலம் | பியூட்டனாயிக் அமிலம் | CH3(CH2)2COOH | வெண்ணெய் |
| 5 | வலேரிக் அமிலம் | பெண்டனாயிக் அமிலம் | CH3(CH2)3COOH | வலேரியன் தாவரம் |
| 6 | கேப்ராயிக் அமிலம் | எக்சனாயிக் அமிலம் | CH3(CH2)4COOH | கொழுப்பு |
| 7 | எனான்திக் அமிலம் | எப்டனாயிக் அமிலம் | CH3(CH2)5COOH | |
| 8 | கேப்ரைலிக் அமிலம் | Oஆக்டனாயிக் அமிலம் | CH3(CH2)6COOH | தாய்ப்பால், தேங்காய் |
| 9 | பெலார்கோனிக் அமிலம் | நோனானாயிக் அமிலம் | CH3(CH2)7COOH | |
| 10 | கேப்ரிக் அமிலம் | டெக்கனாயிக் அமிலம் | CH3(CH2)8COOH | தேங்காயெண்னெய் |
| 11 | அன்டெசைலிக் அமிலம் | அன்டெக்கனாயிக் அமிலம் | CH3(CH2)9COOH | |
| 12 | லாரிக் அமிலம் | டைடெக்கனாயிக் அமிலம் | CH3(CH2)10COOH | தேங்காயெண்ணெய் |
| 13 | டிரைடெசைலிக் அமிலம் | டிரைடெக்கனாயிக் அமிலம் | CH3(CH2)11COOH | |
| 14 | மிரிசுடிக் அமிலம் | டெட்ராடெக்கனாயிக் அமிலம் | CH3(CH2)12COOH | சாதிக்காய் |
| 15 | பென்டாடைசிலிக் அமிலம் | பென்டாடெக்கனாயிக் அமிலம் | CH3(CH2)13COOH | |
| 16 | பால்மிடிக் அமிலம் | எக்சாடெக்கனாயிக் அமிலம் | CH3(CH2)14COOH | பாமாயில் |
| 17 | மார்காரிக் அமிலம் | எப்டாடெக்கனாயிக் அமிலம் | CH3(CH2)15COOH | |
| 18 | சிடீயரிக் அமிலம் | ஆக்டாடெக்கனாயிக் அமிலம் | CH3(CH2)16COOH | சாக்கலேட்டு மெழுகு |
| 19 | நோனாடெசைலிக் அமிலம் | நோனோடெக்கனாயிக் | CH3(CH2)17COOH | கொழுப்பு, எண்ணெய் |
| 20 | அராசிடிக் அமிலம் | ஐகோசனாயிக் அமிலம் | CH3(CH2)18COOH | கடலை எண்ணெய் |
| சேர்ம வகை | உறுப்பினர்கள் |
|---|---|
| நிறைவுறா மோனோகார்பாக்சிலிக் அமிலங்கள் | அக்ரைலிக் அமிலம் அல்லது 2-புரோப்பனாயிக் அமிலம்– CH2=CHCOOH, பலபடி தயாரித்தலில் பயன்படுகிறது |
| கொழுப்பு அமிலங்கள் | நிரைவுற்ற நீன்ட சங்கிலி மற்ரும் நிறைவுறா மோனோகார்பாக்சிலிக் அமிலங்கள், ஊட்டச்சத்துப் பொருளாக |
| அமினோ அமிலங்கள் | புரோட்டின் கட்டுறுப்புகள் |
| கீட்டோ அமிலங்கள் | உயிர்வேதியியல் முக்கியத்துவம் கொண்டவை, கீட்டோன் குழுவைக் கொண்டிருக்கும் உதாரணம் அசிட்டோ அசிட்டிக் அமிலம், பைரூவிக் அமிலம் |
| அரோமாட்டிக் கார்பாக்சிலிக் அமிலங்கள் | பென்சாயிக் அமிலம், உணவுப் பாதுகாப்பு |
| டைகார்பாக்சிலிக் அமிலங்கள் | இரண்டு கார்பாக்சில் குழுக்கள் இருக்கும். உதாரணம் அடிப்பிக் அமிலம் – சர்க்கரை அமிலக் குடும்பம் |
| டிரைகார்பாக்சிலிக் அமிலங்கள் | மூன்று கார்பாக்சில் குழுக்கள் இருக்கும் உதாரணம் சிட்ரிக் அமிலம்] – சிட்ரசு வகை பழங்களில் இருக்கும் |
| ஆல்பா ஐதராக்சி அமிலங்கள் | ஐதராக்சி குழுவைக் கொண்டுள்ளது. கிளைசரிக் அமிலம், கிளைக்காலிக் அமிலம், லாக்டிக் அமிலம் போன்றவை டார்டாரிக் அமிலத்தில் உள்ளது |
| டைவினைல்யீத்தர் கொழுப்பு அமிலங்கள் | இரட்டை நிறைவுறா கார்பன் சங்கிலி ஈதர் பிணைப்பின் வழியாக, சில தாவரங்களில் உள்ளது |
கார்பாக்சிலிக் தனியுறுப்பு
தனியுறுப்பு •COOH (CAS# 2564-86-5) நிலைப்புத்தன்மை குறைவாகக் கொண்டது [3] ஆகும். எலக்ட்ரான் நிலைகாந்த ஒத்திசைவு நிறமாலை முறையில் அமிலப் பிரிகை மாறிலி கணக்கிடப்படுகிறது [4]. கார்பாக்சில் குழு இருபடியாக்கலுக்கு உட்பட்டு ஆக்சாலிக் அமிலமாக உருவாகிறது.
இயற்பியல் பண்புகள்
கரைதிறன்
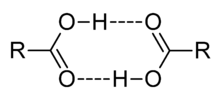
கார்பாக்சிலிக் அமிலங்கள் முனைவுற்றவை ஆகும். ஏனென்றால் அவை ஐதரசன் பிணைப்பு ஏற்பிகள் (கார்பனைல் -–C=O) மற்றும் ஐதரசன் பிணைப்பு வழங்கிகள் (ஐதராக்சில் –OH) ஆகிய இரண்டுமாகச் செயல்படுகின்றன. மேலும் இவை ஐதரசன் பிணைப்பில் பங்கேற்கின்றன. கார்பாக்சில் மற்றும் கார்பனைல் குழுக்கள் இரண்டும் சேர்ந்து கார்பாக்சில் வேதிவினைக் குழு உருவாகிறது. கார்பாக்சிலிக் அமிலங்கள் வழக்கமாக தன்னியக்கத்தைக் கொண்டிருப்பதால் பொதுவாக இவை இருபடி இணைகளாக முனைவற்ற ஊடகங்களில் கானப்படுகின்றன. 1 முதல் 5 வர கார்பன் எண்ணிக்கை கொண்ட சிறிய கார்பாக்சிலிக் அமிலங்கள் தண்ணீரில் கரைகின்றன. உயர் கார்பாக்சிலிக் அமிலங்கள் தண்ணீரில் குறைவாகக் கரைகின்றன. ஆனால் ஈதர், ஆல்ககால் போன்ற குறை முனைவு கரைப்பான்களில் இவை கரைகின்றன [5].
கொதிநிலை
கார்பாக்சிலிக் அமிலங்கள் தண்ணீரைவிட அதிக கொதிநிலையை கொண்டிருக்கின்றன, அவற்றின் அதிகரித்த மேற்பரப்புப் பகுதி மட்டும் இதற்கு காரணமல்ல அவை நிலையான இருபடிகளாக உருவாக்குகின்ற அவற்றின் போக்கும் ஒரு காரணமாக இருக்கின்றது. கார்பாக்சிலிக் அமிலங்கள் இந்த இருபடிகளாக ஆவியாகவோ அல்லது கொதிக்கவோ செய்கின்றன. கொதிநிலை ஏற்படுவதற்கு இவற்றி இருபடி பிணைப்புகளும் உடைக்கப்பட வேண்டும் அல்லது முழுமையான இருபடியும் ஆவியாக்கம் செய்யப்பட வேண்டும். இவ்விரண்டுமே ஆவியாதல் வெப்பத்தின் தேவைகளை அதிகரிக்கும்.
அமிலத்தன்மை
கார்பாக்சிலிக் அமிலங்கள் பிரான்சுடெட்டு-லவ்ரி அமிலங்களாகும். ஏனெனில் அவை புரோட்டான் (H+) வழங்கிகளாகும். இவை பொதுவான கரிம அமிலங்களாகக் கருதப்படுகின்றன. கார்பாக்சிலிக் அமிலங்கள் பொதுவாக பலவீனமான அமிலங்களாக இருக்கின்றன, அதாவது, அவை நடுநிலையான நீர்த்த கரைசல்களில் பகுதியாக மட்டுமே பிரிகை அடைந்து H + நேர்மின் அயனிகளாகவும் RCOO- எதிர்மின் அயனிகளாகவும் பிரிகின்றன. உதாரணமாக, அறை வெப்பநிலையில் 1-மோலார் அசிட்டிக் அமிலத்தின் கரைசலில், அமில மூலக்கூறுகளில் 0.4% அமில மூலக்கூறுகள் மட்டுமே பிரிக்கப்படுகின்றன. மின்னெதிர் பதிலீடுகள் வலுவான அமிலங்களை வழங்குகின்றன.
| கார்பாக்சிலிக் அமிலம்[6] | pKa |
|---|---|
| அசிட்டிக் அமிலம் (CH3CO2H) | 4.76 |
| பென்சாயிக் அமிலம் (C6H5CO2H) | 4.2 |
| பார்மிக் அமிலம் (HCOOH) | 3.75 |
| குளோரோ அசிட்டிக் அமிலம் (CH2ClCO2H) | 2.86 |
| டைகுளோரோ அசிட்டிக் அமிலம் (CHCl2CO2H) | 1.29 |
| ஆக்சாலிக் அமிலம் (HO2CCO2H) | 1.27 |
| டிரைகுளோரோ அசிட்டிக் அமிலம் (CCl3CO2H) | 0.65 |
| டிரைபுளோரோ அசிட்டிக் அமிலம் (CF3CO2H) | 0.23 |
நெடி
கார்பாக்சிலிக் அமிலங்கள் குறிப்பாக ஆவியாகும் பெறுதிகள் பெரும்பாலும் கடுமையான நெடியைக் கொண்டுள்ளன. பொதுவாக அசிட்டிக் அமிலம் மற்றும் பியூட்டைரிக் அமிலம் போன்றவை உதாரணங்களாகும். கார்பாக்சிலிக் அமிலங்களின் எசுத்தர்கள் இனிமையான மணம் கொண்டவையாக உள்ளன. வாசனை திரவியங்களிலும் பயன்படுத்தப்படுகின்றன.
அடையாளம் காணல்
அகச்சிவப்பு நிறமாலையியல் ஆய்வு மூலம் கார்பாக்சிலிக் அமிலங்கள் உடனடியாக அடையாளம் காணப்படுகின்றன. 1680 மற்றும் 1725 சென்டிமீட்டர் அலைவரிசையில் அவை C-O அதிர்வு பிணைப்பு (νC = O) உடன் தொடர்புடைய ஒரு கூர்மையான கற்றையாக வெளிப்படுகின்றன. தனித்தன்மை மிக்க νO–H கற்றை 2500- 3000 செ,மீ−1 பகுதி மண்டலத்தில் வெளிப்படுகிறது. 1H அணுக்கரு காந்த ஒத்திசைவு நிறமாலையில் மில்லியனுக்கு 10-13 பகுதி மண்டலத்தில் ஐதராக்சிலின் ஐதரசன் தோன்றுகிறது.
தோற்றமும் பயன்பாடுகளும்
தொழில் முறையாக பல கார்பாக்சிலிக் அமிலங்கள் பெருமளவில் தயாரிக்கப்படுகின்றன. இயற்கையிலும் எங்கும் இவை பரவியுள்ளன. கொழுப்பு அமிலங்களின் எசுத்தர்கள் லிப்பிடுகளின் முக்கியமான பகுதிப் பொருளாகும். அமினோகார்பாக்சிலிக் அமிலங்களின் பாலி அமைடுகள் புரதங்களின் பிரதானமான பகுதிப் பொருளாகும். பலபடிகள், மருந்துகள், கரைப்பான்கள், உணவுகூட்டுப் பொருள்கள் போன்றவை தயாரிப்பில் கார்பாக்சிலிக் அமிலங்கள் பெரிதும் பயன்படுகின்றன. அசிட்டிக் அமிலம், அக்ரைலிக் அமிலம், மெத்தக்ரைலிக் அமிலம், அடிப்பிக் அமிலம், சிட்ரிக் அமிலம்,, கொழுப்பு அமிலங்கள், புரோப்பியானிக் அமிலம், ம்லேயிக் அமிலம் போன்ற பல கார்பாக்சிலிக் அமிலங்கள் வர்த்தக முக்கியத்துவம் பெற்றவையாக உள்ளன.
மேற்கோள்கள்
- தனி மற்றும் பயன்பாட்டு வேதியியல் அனைத்துலக ஒன்றியம். "carboxylic acids". Compendium of Chemical Terminology Internet edition.
- Recommendations 1979. Organic Chemistry IUPAC Nomenclature. Rules C-4 Carboxylic Acids and Their Derivatives.
- Milligan, D. E.; Jacox, M. E. (1971). "Infrared Spectrum and Structure of Intermediates in Reaction of OH with CO". Journal of Chemical Physics 54 (3): 927–942. doi:10.1063/1.1675022. Bibcode: 1971JChPh..54..927M.
- The value is pKa = −0.2 ± 0.1. Jeevarajan, A. S.; Carmichael, I.; Fessenden, R. W. (1990). "ESR Measurement of the pKa of Carboxyl Radical and Ab Initio Calculation of the Carbon-13 Hyperfine Constant". Journal of Physical Chemistry 94 (4): 1372–1376. doi:10.1021/j100367a033.
- Morrison, R.T.; Boyd, R.N. (1992). Organic Chemistry (6th ). பன்னாட்டுத் தரப்புத்தக எண்:0-13-643669-2.
- Haynes, William M., தொகுப்பாசிரியர் (2011). CRC Handbook of Chemistry and Physics (92nd ). CRC Press. பக். 5–94 to 5–98. பன்னாட்டுத் தரப்புத்தக எண்:1439855110.