ব্রাইনের তড়িৎবিশ্লেষণ
ক্লোর্যালক্যালি পদ্ধতি (ক্লোর-এলক্যালি) হচ্ছে সোডিয়াম ক্লোরাইডের তড়িৎবিশ্লেষণের জন্য ব্যবহৃত একটি রাসায়নিক পদ্ধতি। শিল্প কারাখানায় বহুল ব্যবহৃত রাসায়নিক সোডিয়াম হাইড্রোক্সাইড (কস্টিক সোডা) এবং ক্লোরিন গ্যাস উৎপাদনে এই পদ্ধতি ব্যবহার করা হয়। ১৯৮৭ সালে এই পদ্ধতি ব্যবহার করে ৩৫ মিলিয়ন টন ক্লোরিন গ্যাস উৎপাদন করা হয়।
সাধারনত এই পদ্ধতি সোডিয়াম ক্লোরাইডের জলীয় দ্রবন ব্রাইনের উপর পরিচালিত করা হয় এবং ফলশ্রুতিতে সোডিয়াম হাইড্রোক্সাইড, হাইড্রোজেন এবং ক্লোরিন গ্যাস উৎপন্ন হয়। সোডিয়াম ক্লোরাইডের এর বদলে ক্যালসিয়াম ক্লোরাইড বা পটাশিয়াম ক্লোরাউড ব্যবহার করলে ক্যালসিয়াম বা পটাশিয়ামের হাইড্রোক্সাইড উৎপন্ন হবে।
এই পদ্ধতিতে বিপুল পরিমানে শক্তি খরচ হয়। উদাহরণ হিসেবে বলা যায় ১৯৮৫ সালে পশ্চিম জার্মানীতে ৪ বিলিয়ন kWh এর বেশি শক্তি ব্যবহার করা হয়েছে।[1] এই পদ্ধতি সম সংখ্যক মোলার ক্লোরিন গ্যাস এবং সোডিয়াম হাইড্রোক্সাইড উৎপন্ন করে। ক্লোরিন গ্যাস বিষাক্ত। এই গ্যাসকে বাতাসে ছেড়ে দেয়ার উপায় নেই। সেজন্য ক্লোরিন গ্যাস ব্যবহারের উপযুক্ত পথ খুঁজে নিতে হয়।
পদ্ধতিসমূহ
তিনটি উৎপাদন পদ্ধতি ব্যবহার করা হয়। মার্কারি-সেল পদ্ধতিতে ক্লোরিন মুক্ত সোডিয়াম হাইড্রোক্সাইড উৎপন্ন হয় কিন্তু টন টন মার্কারি ব্যবহারের ফলে পরিবেশগত সমস্যা দেখা দেয়। সাধারণ পদ্ধতিতে প্রতিবছর কয়েকশত পাউন্ড মার্কারি বাতাসে মিশে যায়। অন্যদিকে মার্কারি সেলে উৎপাদিত ক্লোরিন এবং কস্টিক সডার সাথে সামান্য পরিমানে মার্কারি মিশে থাকে। বর্তমানে কস্টিক সোডা উৎপাদনে মেমব্রেন সেল পদ্ধতি বহুল ব্যবহৃত হচ্ছে।
মেমব্রেন সেল
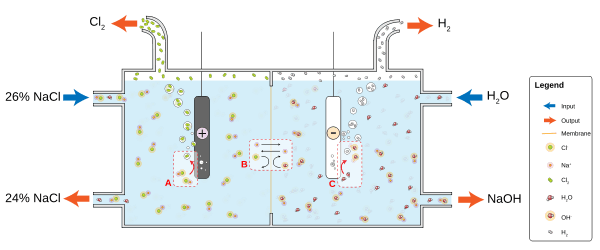
মেমব্রেন সেলে সোডিয়াম হাইড্রোক্সাইড উৎপাদনের জন্য সোডিয়াম ক্লোরাইডের জলীয় দ্রবনকে তড়িৎ বিশ্লেষণ করা হয়।
ব্রাইনের সম্পৃক্ত দ্রবণকে একটি প্রকোষ্ঠে প্রেরণ করা হয় যেখানে ক্লোরাইড আয়ন এনোডে জারিত হয়, ইলেকট্রন হারিয়ে ক্লোরিন গ্যাস তৈরী করেঃ
- 2Cl− → Cl
2 + 2e−
ক্যাথোডে পানি থেকে উৎপন্ন ধনাত্বক হাইড্রোজেন আয়ন হাইড্রোজেন গ্যাস এবং হাইড্রোক্সাইড আয়ন উৎপন্ন করেঃ
- 2H
2O + 2e− → H2 + 2OH−
মেমব্রেন সেলের মেমব্রেনটি আয়ন ভেদী এজন্য একে আয়ন-এক্সচেঞ্জ মেমব্রেন বলে। এই মেমব্রেন সোডিয়াম আয়নকে (Na+) অপরপার্শ্বে যেতে দেয় যেখানে হাইড্রোক্সাইড আয়নের সাথে বিক্রিয়া করে কস্টিক সোডা (NaOH) প্রস্তুত করে। ব্রাইনের তড়িৎবিশ্লেষণের সামগ্রিক বিক্রিয়াটি নিম্নরূপঃ
- 2NaCl + 2H
2O → Cl
2 + H
2 + 2NaOH
ক্লোরিন এবং হাইড্রোজেন আয়নকে আলাদা রাখতেই মেমব্রেন সেল ব্যবহার করা হয়। কারণ ক্লোরিন এবং হাইড্রোজেন আয়ন পরষ্পরের সংস্পর্ষে এলে ক্লোরাইড এবং হাইপোক্লোরাইট আয়ন গঠন করেঃ
- Cl
2 + 2OH− → Cl− + ClO− + H
2O
60 °C এর বেশি তাপমাত্রায় ক্লোরেট গঠন করেঃ
- 3Cl
2 + 6OH− → 5Cl− + ClO
3− + 3H
2O
ক্লোরিন ক্ষয়কারক সেজন্য এনোড (যেখানে ক্লোরিন উৎপন্ন হয়) অবশ্যই ক্ষয়রোধী, অবিক্রিয়ক ধাতু যেমন টাইটেনিয়াম দিয়ে তৈরী হতে হবে। অন্যদিকে ক্যাথোড (যেখানে হাইড্রোক্সাইড গঠিত হয়) সহজে জারিত হয় এমন ধাতু যেমন নিকেল দিয়ে তৈরী করা যাবে।
মেমব্রেন সেলে এনোড এবং ক্যাথোড আয়নভেদী মেমব্রেন দ্বারা আলাদা করা থাকে। এই পুরো প্রক্রিয়াকে একত্রে ইলেকট্রোলাইজার বলে। একটি ইলেকটোলাইজারে একাধিক সেল থাকে। সেক্ষেত্রে এনোড এবং ক্যাথোডের সমন্বয়ে বাইপোলার ফ্রেম ব্যবহার করা হয়। দুটি ফ্রেমের মাঝে মেমব্রেনকে স্থাপন করা হয়। স্যাচুরেটেড ব্রাইন (সোডিয়াম ক্লোরাইডের সম্পৃক্ত দ্রবণ) এনোড অংশে এসিড সহ প্রবেশ করানো হয়। একে এনোলাইট বলা হয়। DC কারেন্ট রেক্টিফায়ারের মাধ্যমে ইলেকট্রোলাইজারের মাধ্যমে পরিচালিত করা হয়। NaCl এর উপাদানে ভেঙে যায়। কিন্তু মেমব্রেন শুধু মাত্র Na+ আয়নকে অপরপার্শ্বে যেতে দেয়। সেখানে উৎপন্ন হাইড্রোক্সাইড আয়নের সাথে মিলিত হয়ে কস্টিক সোডা উৎপন্ন করে। এনোডে ক্লোরাইড আয়ন জারিত হয়ে ক্লোরিন গ্যাস গঠন করে এবং ক্যাথোডে হাইড্রোজেন গ্যাস গঠিত হয়। উৎপন্ন হাইড্রোজেন এবং ক্লোরিন গ্যাসকে উচ্চতাপে হাইড্রোক্লোরিক এসিড গঠন করে। ক্লোরিণ গ্যাসকে তরলীকরণ করে সিলিন্ডারে করে বাজারজাত করা হয়।
মেমব্রেন সেল পদ্ধতিতে পরিবেশ দূষণের মাত্রা অপেক্ষাকৃত কম বলে বাংলাদেশ, জাপানসহ বিশ্বের বিভিন্ন দেশে এই পদ্ধতিতে কস্টিক সোডা উৎপাদন করা হয়।
ডায়াফ্রাম সেল
ডায়াফ্রেম সেল পদ্ধতিতে দুই প্রকোষ্ঠকে একটি ভেদ্য ডায়াফ্রাম যা দ্বারা আলাদা করা হয়। ডায়াফ্রাম সাধারনত এসবেস্টস দিয়ে তৈরী করা হয়। ব্রাইন এনোড কম্পার্টমেন্টে প্রবেশ করানো হয় এবং এখান থেকে ক্যাথোড কম্পার্টমেন্টে প্রবাহিত হয়। মেমব্রেন সেলের মত এনোডে ক্লোরাইড আয়ন জারিত হয়ে ক্লোরিন তৈরী করে, পানি ভেঙে কস্টিক সোডা ও হাইড্রোজেন তৈরী করে। ডায়াফ্রাম কস্টিক সোডা এবং ক্লোরিন গ্যাসকে পরষ্পরের সংস্পর্শে আসা থেকে বিরত রাখে।
সেল থেকে পাতলা কস্টিক ব্রাইন বেরিয়ে আসে। লবনকে আলাদা করা হয়। ইভাপোরেটর ব্যবহার করে কস্টিক সোডাকে সাধারনত ৫০% ঘনত্বে রূপান্তর করা হয়। এটা করতে প্রতি টন কস্টিকের জন্য তিন টন বাষ্প ব্যবহার করা হয়। কস্টিক ব্রাইন থেকে আলদা করা লবন পূনরায় সম্পৃক্ত ব্রাইন হিসেবে ব্যবহার করা হয়। ক্লোরিনের সাথে কিছু অক্সিজেন মিশ্রিত থাকে যা তরলীকরন (লিকুয়েফিকেশান) এবং বাষ্পায়ন (ইভাপোরেশান) পদ্ধতিতে বিশুদ্ধ করা হয়।
মার্কারি সেল
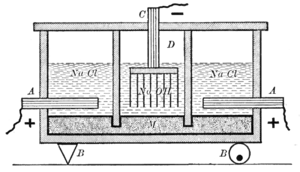
মার্কারি সেল পদ্ধিতি কাস্টনার-কেলনার পদ্ধতি নামেও পরিচিত। পারদ বা মার্কারির পাতলা লেয়ার দিয়ে ক্যাথোড প্রস্তুত করা হয়। সম্পৃক্ত ব্রাইন দ্রবন ক্যাথোডের উপর প্রবাহিয় করা হয়। এনোডে ক্লোরিন উৎপন্ন হয়। ক্যাথোডে পারদের সাথে মিলিত হয়ে সোডিয়াম-মার্কারি এমালগাম হিসেবে সোডিয়াম উৎপন্ন হয়।
এমালগাম সেল থেকে বের করে আনা হয় এবং পানির সাথে বিক্রিয়া করানো হয়। এমালগাম ভেঙে সোডিয়াম হাইড্রোক্সাইড এবং মার্কারি গঠন করে। মার্কারিকে পূনরায় ইলেকট্রোলাইট সেলে ব্যবহার করা যায়। মার্কারির ক্ষতিকর প্রভাবে পরিবেশ দূষণ হয়। কানাডা এবং জাপানে এর ব্যাপক ক্ষতিকর প্রভাব দেখা দেয়। বাংলাদেশের প্রথম কস্টিক উৎপাদনকারী প্লান্ট চট্টগ্রাম কেমিক্যালস মার্কারি সেল পদ্ধতিতে কস্টিক উৎপাদন করতো। পরবর্তিতে মার্কারি ব্যবহারে নিষেদ্ধাজ্ঞা জারী করা হয়।
উৎপাদনকারীদের সংগঠন
কস্টিক সোডার গুরুত্বের ভিত্তিতে আঞ্চলিক জাতীয়, আন্তঃর্জাতিক পর্যায়ে বেশ কিছু সংগঠন গড়ে উঠেছে। ইউরো ক্লোর এবং দ্যা ওয়ার্ল্ড ক্লোরিন কাউন্সিল এরকমই দুটো প্রতিষ্ঠান।
ল্যাবরেটরি পদ্ধতি
দুটি বিকার ব্যবহার করে তড়িৎ বিশ্লেষণ করা যায়। একটি বিকারে থাকবে ব্রাইন দ্রবণ এবং অন্যটিতে বিশুদ্ধ পানি। দুই বিকারকে সংযুক্ত করতে সল্ট ব্রিজ বা লবন সেতু তৈরী করতে হবে। একটি বাঁকানো হোস পাইপ দিয়ে দুই বিকারকে সংযোগ করতে হবে। ধাতব বল ব্যবহার করা উচিত নয়। শেষ মাথা টিস্যু অথবা কাপড় দিয়ে আঁটকে দিতে হবে। যে বিকারে সোডিয়াম হাইড্রোক্সাইড এবং হাইড্রোজেন উৎপাদন করতে চাই সেখানে ঋনাত্বক ইলেকট্রড প্রবেশ করাতে হবে। অন্যটিতে কার্বন দন্ড দিয়ে প্রস্তুত ধনাত্বক ইলেকট্রোড প্রবেশ করাতে হবে।
১২ ভোল্টের ব্যাটারির সাহায্যে দুই তড়িৎদ্বারকে সংযুক্ত করতে হবে। এনোডে ক্লোরিন এবং ক্যাথোডে সোডিয়াম হাইড্রোক্সাইড উৎপন্ন হবে।
তথ্য উৎস
- হলম্যান, এ. এফ.; উইবার্গ, সি. (২০০১), ইনঅরগেনিক কেমিস্ট্র, সান ডিয়াগো: অ্যাকাডেমিক প্রেস, আইএসবিএন 0-12-352651-5
আরো পড়ুন
- Bommaraju, Tilak V.; Orosz, Paul J.; Sokol, Elizabeth A.(2007). "Brine Electrolysis." Electrochemistry Encyclopedia. Cleveland: Case Western Rsserve University.