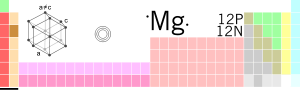ಮೆಗ್ನೀಸಿಯಮ್
ಮೆಗ್ನೀಶಿಯಂ ಒಂದು ಮೂಲಧಾತು ಲೋಹ. ಇದನ್ನು Mg ಚಿಹ್ನೆಯಿಂದ ಗುರುತಿಸಬಹುದು ಮತ್ತು ಇದರ ಪರಮಾಣು ಸಂಖ್ಯೆ 12. ಇದನ್ನು ೧೮೩೧ರಲ್ಲಿ ಸರ್ ಹಂಫ್ರಿ ಡೇವಿ ಮೊದಲ ಬಾರಿಗೆ ಶುದ್ಧ ರೂಪದಲ್ಲಿ ಪ್ರತ್ಯೇಕಿಸಿದರು. ಇದನ್ನು ಮಿಶ್ರ ಲೋಹಗಳ ಉತ್ಪಾದನೆಯಲ್ಲಿ ಮತ್ತು ಎಲೆಕ್ಟ್ರಾನಿಕ್ಸ್ ಉಪಕರಣಗಳಲ್ಲಿ ಹೆಚ್ಚು ಬಳಸಲಾಗುತ್ತದೆ. ಇದು ಬೆಳ್ಳಿಯ ಹೊಳಪುಳ್ಳ ಅತ್ಯಂತ ಹಗುರವಾದ, ಅಲ್ಯುಮಿನಿಯಮ್ ಗಿಂತ ಹೆಚ್ಚು ಕಠಿಣವಾದುದು ಮತ್ತು ಬಲವಾದುದು. ಈ ಲೋಹವು ತಂತುರೂಪಕತ್ವ ಮತ್ತು ಪತ್ರರೂಕ್ಷಮತ್ವಗಳನ್ನು ಹೊಂದಿದ್ದು ಇದನ್ನು ಯಂತ್ರಗಳಿಂದ ಕಡೆದು ಅಪೇಕ್ಷಿತ ಆಕಾರವನ್ನು ಇದಕ್ಕೆ ಕೊಡಬಹುದು. ರಾಸಾಯನಿಕವಾಗಿ ಸಾಮಾನ್ಯ ಶಾಖಗಳಲ್ಲಿ ತೇವದಿಂದ ಕೂಡಿದ ಗಾಳಿಯಲ್ಲಿಯೂ ಇದು ದೃಡವಾಗಿರುವುದು. ಈ ಲೋಹವನ್ನು ಗಾಳಿಯಲ್ಲಿ ಕಾಯಿಸಿದರೆ, ಕಣ್ಣು ಕುಕ್ಕುವ ಜ್ವಾಲೆಯಿಂದ ಉರಿದು, ಆಕ್ಸೈಡ್ ಮತ್ತು ನೈಟ್ರೈಡ್ ಗಳನ್ನು ಕೊಡುವುದು. ನೀರಿನ ಹಬೆಯು ಕೆಂಗಾವಿಗೆ ಕಾದ ಮೆಗ್ನೀಸಿಯಮ್ ನ ಮೇಲೆ ವರ್ತಿಸಿ ಅದನ್ನು ಮೆಗ್ನೀಸಿಯಮ್ ಆಕ್ಸೈಡಿಗೆ ಪರಿವರ್ತಿಸುವುದು ಮತ್ತು ಹೈಡ್ರೊಜನ್ ಬಿಡುಗಡೆಯಾಗುವುದು.
- 3Mg + N2 → Mg3N2
- 2Mg + O2 → 2MgO
- Mg + H2O → MgO + H2
| |||||||||||||||
| ಸಾಮಾನ್ಯ ಮಾಹಿತಿ | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ಹೆಸರು, ಚಿಹ್ನೆ ಮತ್ತು ಕ್ರಮಾಂಕ | ಮ್ಯಗ್ನೀಶಿಯಮ್, Mg, ೧೨ | ||||||||||||||
| ರಾಸಾಯನಿಕ ಸರಣಿ | alkaline earth metal | ||||||||||||||
| ಗುಂಪು, ಆವರ್ತ, ಖಂಡ | 2, 3, s | ||||||||||||||
| ಸ್ವರೂಪ | ಬೆಳ್ಳಿಯಂತಹ ಬಿಳಿ ಬಣ್ಣ | ||||||||||||||
| ಅಣುವಿನ ತೂಕ | 24.3050(6) g·mol−1 | ||||||||||||||
| ಋಣವಿದ್ಯುತ್ಕಣ ಜೋಡಣೆ | [Ne] 3s2 | ||||||||||||||
| ಋಣವಿದ್ಯುತ್ ಪದರಗಳಲ್ಲಿ ಋಣವಿದ್ಯುತ್ಕಣಗಳು | 2, 8, 2 | ||||||||||||||
| ಭೌತಿಕ ಗುಣಗಳು | |||||||||||||||
| ಹಂತ | solid | ||||||||||||||
| ಸಾಂದ್ರತೆ (ಕೋ.ತಾ. ಹತ್ತಿರ) | 1.738 g·cm−3 | ||||||||||||||
| ದ್ರವದ ಸಾಂದ್ರತೆ at ಕ.ಬಿ. | 1.584 g·cm−3 | ||||||||||||||
| ಕರಗುವ ತಾಪಮಾನ | 923 K (650 °C, 1202 °ಎಫ್) | ||||||||||||||
| ಕುದಿಯುವ ತಾಪಮಾನ | 1363 K (1091 °C, 1994 °F) | ||||||||||||||
| ಸಮ್ಮಿಲನದ ಉಷ್ಣಾಂಶ | 8.48 kJ·mol−1 | ||||||||||||||
| ಭಾಷ್ಪೀಕರಣ ಉಷ್ಣಾಂಶ | 128 kJ·mol−1 | ||||||||||||||
| ಉಷ್ಣ ಸಾಮರ್ಥ್ಯ | (25 °C) 24.869 J·mol−1·K−1 | ||||||||||||||
| |||||||||||||||
| ಅಣುವಿನ ಗುಣಗಳು | |||||||||||||||
| ಸ್ಪಟಿಕ ಸ್ವರೂಪ | hexagonal | ||||||||||||||
| ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಗಳು | 2, 1 (strongly basic oxide) | ||||||||||||||
| ವಿದ್ಯುದೃಣತ್ವ | 1.31 (Pauling scale) | ||||||||||||||
| ಅಣುವಿನ ತ್ರಿಜ್ಯ | 150 pm | ||||||||||||||
| ಅಣುವಿನ ತ್ರಿಜ್ಯ (ಲೆಖ್ಕಿತ) | 145 pm | ||||||||||||||
| ತ್ರಿಜ್ಯ ಸಹಾಂಕ | 130 pm | ||||||||||||||
| ವಾನ್ ಡೆರ್ ವಾಲ್ಸ್ ತ್ರಿಜ್ಯ | 173 pm | ||||||||||||||
| ಇತರೆ ಗುಣಗಳು | |||||||||||||||
| ಕಾಂತೀಯ ವ್ಯವಸ್ಥೆ | paramagnetic | ||||||||||||||
| ವಿದ್ಯುತ್ ರೋಧಶೀಲತೆ | (20 °C) 43.9 nΩ·m | ||||||||||||||
| ಉಷ್ಣ ವಾಹಕತೆ | (300 K) 156 W·m−1·K−1 | ||||||||||||||
| ಉಷ್ಣ ವ್ಯಾಕೋಚನ | (25 °C) 24.8 µm·m−1·K−1 | ||||||||||||||
| ಶಬ್ದದ ವೇಗ (ತೆಳು ಸರಳು) | (r.t.) (annealed) 4940 m·s−1 | ||||||||||||||
| ಯಂಗ್ನ ಮಾಪನಾಂಕ | 45 GPa | ||||||||||||||
| ವಿರೋಧಬಲ ಮಾಪನಾಂಕ | 17 GPa | ||||||||||||||
| ಸಗಟು ಮಾಪನಾಂಕ | 45 GPa | ||||||||||||||
| ವಿಷ ನಿಷ್ಪತ್ತಿ | 0.29 | ||||||||||||||
| ಮೋಸ್ ಗಡಸುತನ | 2.5 | ||||||||||||||
| ಬ್ರಿನೆಲ್ ಗಡಸುತನ | 260 MPa | ||||||||||||||
| ಸಿಎಎಸ್ ನೋಂದಾವಣೆ ಸಂಖ್ಯೆ | 7439-95-4 | ||||||||||||||
| ಉಲ್ಲೇಖನೆಗಳು | |||||||||||||||
ಮೆಗ್ನೀಶಿಯಂ ಲಭ್ಯತೆ
ಭೂಪದರದ ಶೇಕಡ 2.5 ಭಾಗವಿರುವ ಈ ಮೂಲವಸ್ತುವು ಅತ್ಯಂತ ವಿಸ್ತೃತವಾಗಿ ಹರಡಿರುವ ಮೂಲವಸ್ತುಗಳ ಪೈಕಿ ಒಂದು. ಮೆಗ್ನೀಸಿಯಮ್ ಮೂಲವಸ್ತುವು ಭೂಮಿಯಲ್ಲಿ ಹೇರಳವಾಗಿ ಸಿಗುವ ವಸ್ತುಗಳಲ್ಲಿ ಒಂಬತ್ತನೆಯದ್ದಾಗಿದೆ[1].[2] ಇದನ್ನು ಡಾಲಮೈಟ್, ಮ್ಯಾಗ್ನಸೈಟ್, ಕೀಸರೈಟ್, ಕಾರ್ನಲೈಟ್ ಖನಿಜಗಳಿಂದ ಸಂಸ್ಕರಿಸಬಹುದು. ಮೆಗ್ನೀಸಿಯಮ್ ನ ಅನೇಕ ಸಿಲಿಕೇಟ್ ಗಳೂ ವಿಸ್ತ್ರುತವಾಗಿ ಹರಡಿರುವುವು. ಇವುಗಳ ಪೈಕಿ ಒಲಿರ್ವಿ ((MgFe)2Si2O), ಟಾಲ್ಕ್ (Mg[Si4O10]) ಮುಖ್ಯವಾದವುಗಳು.
ಮೆಗ್ನೀಶಿಯಂ ನ ತಯಾರಿಕೆ
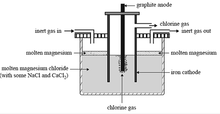
ವಿದ್ಯುದ್ವಿಶ್ಲೇಷಣ ವಿಧಾನ
ಸಾಮಾನ್ಯವಾಗಿ ಕರಗಿಸಿದ ಕಾರ್ನಲೈಟ್ KCl, MgCl2 ಅಥವಾ ಮೆಗ್ನೀಶಿಯಂ ಕ್ಲೋರೈಡ್ ಮತ್ತು ಸೋಡಿಯಂ ಕ್ಲೋರೈಡ್ ಮಿಶ್ರಣವನ್ನು ಕರಗಿಸಿ, ಇದರ ವಿದ್ಯುದ್ವಿಶ್ಲೇಷದಿಂದ ಈ ಲೋಹವನ್ನು ತಯಾರಿಸುವರು. ಹೀಗೆ ಮಿಶ್ರಮಾಡುವ ಕ್ಲೋರೈಡ್ ಗಳ ಪ್ರಮಾಣವು, ಎಲೆಕ್ಟ್ರೋಲೈಟಿಗೆ ಸೂಕ್ತವಾದ ಸಾಂದ್ರತೆ, ಕರಗುವ ಶಾಖ, ವಿದ್ಯುದ್ವಹನತ್ವ ಮೊಂತಾದ ಈ ವಿಧವಾದ ಎಲೆಕ್ಟ್ರೋಲೈಟ್ ಗಳಲ್ಲಿ ಅವಶ್ಯವಾಗಿ ಇರಬೇಕಾದ ಗುಣಗಳನ್ನು ನೀಡಲು ಅಗತ್ಯವಾದಷ್ಟು ಇರಬೇಕು.ವಿದ್ಯುದ್ವಿಶ್ಲೇಷವು ನಡೆಯುವ ಶಾಖದಲ್ಲಿ ಮೆಗ್ನೀಸಿಯಮ್ ಕ್ಲೋರೈಡಿನ ವಿಭಜನೆಯ ವೋಲ್ಟೇಜು ಅತ್ಯಂತ ಕೆಳಮಟ್ಟದ್ದಾಗಿದ್ದು, ಮೆಗ್ನೀಶಿಯಂ ಕ್ಲೋರೈಡು ಮಾತ್ರ ವಿಭಜಿಸಿ ಇತರ ಕ್ಲೋರೈಡುಗಳು ವಿಭಜಿಸದೆ ಇರುವಂತಹ ಮಟ್ಟದಲ್ಲಿ ವೋಲ್ಟೇಜನ್ನು ಯೋಜಿಸುವರು. ವಿದ್ಯುದ್ವಿಶ್ಲೇಷಣಕ್ಕೆ ಅನೇಕ ವಿಧವಾದ ಕೋಶಗಳನ್ನು ಉಪಯೋಗಿಸುವರು.
ಡಾಲಮೈಟ್ ಅಥವಾ ಮ್ಯಾಗ್ನಸೈಟಿನಿಂದ
ಡಾಲಮೈಟ್ ಅಥವಾ ಮ್ಯಾಗ್ನಸೈಟನ್ನು ಕಾಯಿಸುವುದರಿಂದ, ಮೆಗ್ನೀಶಿಯಂ ಆಕ್ಸೈಡ್ ಉಂಟಾಗುವುದು. ಇದನ್ನು ಕಾಯಿಸಿ ಇದರ ಮೇಲೆ ಕಾರ್ಬನ್ ಮಾನಾಕ್ಸೈಡ್ ಮತ್ತು ಕ್ಲೋರೀನಿನ ಮಿಶ್ರಣವನ್ನು ಹಾಯಿಸುವರು.
- MgO + C + Cl2 → MgCl2 + CO
ಸಮುದ್ರದ ನೀರಿನಿಂದ
ಸಮುದ್ರದ ನೀರನ್ನು ಪರಿವರ್ತೆನೆಯ ತೊಟ್ಟಿಗಳಿಗೆ ಪಂಪ್ ಮಾಡುವರು. ಇದಕ್ಕೆ ಇದರಲ್ಲಿರುವ ಕ್ಯಾಲ್ಸಿಯಂ ಬೈಕಾರ್ಬೋನೇಟು, ಕ್ಯಾಲ್ಸಿಯಂ ಕಾರ್ಬೋನೇಟ್ ಆಗಲು ಎಷ್ಟು ಸೋಡಿಯಂ ಕಾರ್ಬೋನೇಟು ಬೇಕಾಗುವುದೆಂದು ಲೆಕ್ಕಹಾಕಿ ಅಷ್ಟು ಸೋಡಿಯಂ ಕಾರ್ಬೋನೇಟನ್ನು ತಟ್ಟಿಯೊಳಕ್ಕೆ ಹಾಕುವರು. ಒತ್ತರಿಸಿದ ಕ್ಯಾಲ್ಸಿಯಂ ಕಾರ್ಬೋನೇಟು ತಳವೂರಿದ ಮೇಲೆ, ಇದರಲ್ಲಿ ಇನ್ನು ತಳವೂರದೆ ಇರಬಹುದಾದ ಕ್ಯಾಲ್ಸಿಯಂ ಕಾರ್ಬೋನೇಟನ್ನು ತೆಗೆದು ಹಾಕಲು ಮರಳ ಮೂಲಕ ಇದು ತಿಳಿಯಾದ ಮೇಲೆ ನಿಂತಿರುವ ದ್ರಾವಣವನ್ನು ಶೋಧಿಸುವರು. ಆಮೇಲೆ ಆಯಸ್ಟರ್ ಚಿಪ್ಪುಗಳನ್ನು ಕಾಯಿಸಿ ಪಡೆದ ಶುದ್ಧ ಕ್ಯಾಲ್ಸಿಯಂ ಆಕ್ಸೈಡನ್ನಾಗಲಿ ಅಥವಾ ಡಾಲಮೈಟನ್ನು ಕಾಯಿಸಿ ಪಡೆದ CaO, MgO ಅನ್ನಾಗಲಿ ಹಾಕುವರು. ಮೊದಲಿನ ಸಂದರ್ಭದಲ್ಲಿ, ಒತ್ತರಿಸಿದ ಮೆಗ್ನೀಶಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡು ಪೂರ್ತಿಯಾಗಿ ಸಮುದ್ರದ ನೀರಿನಿಂದ ಬಂದಿರುವುದು. ಎರಡನೆ ಸಂದರ್ಭದಲ್ಲಿ,ಒತ್ತರಿಸಿದ ಮೆಗ್ನೀಶಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡು ಅರ್ಧಭಾಗ ಸಮುದ್ರದ ನೀರಿನಿಂದ, ಇನ್ನರ್ಧ ಭಾಗ ಸುಟ್ಟ ದಾಲಮೈಟಿನಿಂದ ಬಂದಿರುವುದು. ಪರಿವರ್ತನೆಗಳು ಈ ರೀತಿ ಆಗುವುವು.
- MgCl2 + CaO + H2O → Mg(OH)2O + CaCl2
- MgCl2 + (CaO, MgO) + 2H2O → 2Mg(OH)2 + CaCl2
ಇಂಗಾಲ-ಉಷ್ಣವಿಧಾನದಿಂದ ಮೆಗ್ನೀಶಿಯಂ ತಯಾರಿಕೆ (Carbothermal process)
ಈ ವಿಧಾನದಲ್ಲಿ ಎಲೆಕ್ಟ್ರಿಕ್ ಕುಲುಮೆಯಲ್ಲಿ 2000° ಸೆಂ. ನಲ್ಲಿ ಮೆಗ್ನೀಶಿಯಂ ಆಕ್ಸೈಡನ್ನು ಇಂಗಾಲದಿಂದ ಅಪಕರ್ಷಿಸುವರು.[3]
- MgO + CO CO + Mg
ಮೆಗ್ನೀಶಿಯಂ ನ ಉಪಯೋಗಗಳು
- ಎಲೆಕ್ಟ್ರಾನ್ (Elektron) ಎಂಬ ಮಿಶ್ರಲೋಹ ತಯಾರಿಕೆಯಲ್ಲಿ ಮೆಗ್ನೀಶಿಯಂ ಉಪಯೋಗಿಸುತ್ತಾರೆ. ಈ ಮಿಶ್ರಲೋಹದಲ್ಲಿ 9.5% ಅಲ್ಯುಮಿನಿಯಂ, 1.5% ಸತುವು, 0.3% ಮ್ಯಾಂಗನೀಸ್ ಮತ್ತು ಅಲ್ಪ ಪ್ರಮಾಣದಲ್ಲಿ ತಾಮ್ರ ಇರುವುದು. ಈ ಮಿಶ್ರಲೋಹವನ್ನು ವಾಯುಯಾನಗಳಲ್ಲಿ, ಯಾನಗಳ ಚೌಕಟ್ಟುಗಳು, ರೆಕ್ಕೆಗಳು, ನೆಲಕ್ಕಿಳಿಯುವ ಚಕ್ರಗಳು, ಯಂತ್ರಭಾಗಗಳು ಮತ್ತು ಇತರೆ ಸಾಧನ ಸಾಮಾಗ್ರಿಗಳ ತಯಾರಿಕೆಯಲ್ಲಿ ಉಪಯೋಗಿಸುವರು[4][5][6].
- ಆಯುಧಗಳ ಉದ್ಯಮದಲ್ಲಿ, ನೇಯ್ಗೆಯ ಯಂತ್ರಗಳ ಭಾಗಗಳ ತಯಾರಿಕೆಯಲ್ಲಿ, ಕೈಗಾಡಿಗಳ ತಯಾರಿಕೆಯಲ್ಲಿ, ಧಾನ್ಯಗಳನ್ನು ಗೋರುವ ಮೊರಗಳ ತಯಾರಿಕೆಯಲ್ಲಿ ಉಪಯೋಗಿಸುತ್ತಾರೆ.
- ಬಾಣ ಬಿರುಸುಗಳ ತಯಾರಿಕೆಯಲ್ಲಿ, ಫ಼್ಲಾಷ್ ಲೈಟ್ ಛಾಯಾಚಿತ್ರಗ್ರಹಣದಲ್ಲಿ ಮೆಗ್ನೀಶಿಯಂ ಪುಡಿಯನ್ನು ಉಪಯೋಗಿಸುತ್ತಾರೆ.
- ಭೂಮಿಯೊಳಗೆ ಹೋಗಿರುವ ಪೈಪ್ ಲೈನ್ ಮತ್ತು ಹಡಗುಗಳ ತಳಗಳಿಗೆ ಇದನ್ನು ಕ್ಯಾಥೋಡಿಕ್ ರಕ್ಷಕವಾಗಿ ಉಪಯೋಗಿಸುತ್ತಾರೆ.
- ಗ್ರಿಗ್ನಾರ್ಡ್ ಪರಿವರ್ತಕಗಳೆಂಬ ಮುಖ್ಯವಾದ ಒಂದು ಗುಂಪಿಗೆ ಸೇರಿದ ಆರ್ಗ್ಯಾನೊ-ಮೆಗ್ನೀಶಿಯಂ ಸಂಯುಕ್ತಗಳ ಸಂಶ್ಲೇಷಣೆಯಲ್ಲಿ ವಿಶೇಷವಾಗಿ ಬಳಸುವರು.
ಮೆಗ್ನೀಶಿಯಂ ಸಂಯುಕ್ತಗಳು
- ಮೆಗ್ನೀಶಿಯಂ ಆಕ್ಸೈಡ್ (MgO)
- ಮೆಗ್ನೀಶಿಯಂ ಹೈಡ್ರಾಕ್ಸೈಡ್ (MgO(H)2)
- ಮೆಗ್ನೀಶಿಯಂ ಹೈಡ್ರೈಡ್ (MgH2)
- ಮೆಗ್ನೀಶಿಯಂ ನೈಟ್ರೈಡ್ (Mg3N2)
- ಮೆಗ್ನೀಶಿಯಂ ಕಾರ್ಬೊನೇಟ್ (MgCO3)
- ಮೆಗ್ನೀಶಿಯಂ ಕ್ಲೋರೈಡ್ (MgCl2).
ಉಲ್ಲೇಖಗಳು
- Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3rd ed.). Prentice Hall. pp. 305–306. ISBN 978-0131755536.
- Ash, Russell (2005). The Top 10 of Everything 2006: The Ultimate Book of Lists. Dk Pub. ISBN 0-7566-1321-3.
- bo Yang, Cheng; Tian, Yang; Qu, Tao; Yang, Bin. "Production of magnesium during carbothermal reduction of magnesium oxide by differential condensation of magnesium and alkali vapours". Journal of Magnesium and Alloys. ೧ (೪): 323-329. doi:10.1016/j.jma.2014.01.002.
- Dreizin, Edward L.; Berman, Charles H.; Vicenzi, Edward P. (2000). "Condensed-phase modifications in magnesium particle combustion in air". Scripta Materialia. 122: 30–42. doi:10.1016/S0010-2180(00)00101-2
- Dorr, Robert F (15 September 2012). Mission to Tokyo: The American Airmen Who Took the War to the Heart of Japan. pp. 40–41. ISBN 9781610586634
- AAHS Journal. 44–45. American Aviation Historical Society. 1999