புளுட்டோனியம்
புளுட்டோனியம் (Plutonium) என்பது Pu என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமகும். புளுட்டோனியத்தின் அணு எண் 94 ஆகும். கதிரியக்கத் தனிமமான இது வெள்ளிய சாம்பல் நிற தோற்றத்தில் உள்ளது. காற்றில் பட நேர்ந்தால் ஆக்சிசனேற்றம் அடைந்து மங்கலான மேலுறை உருவாகி ஒளி மங்கிப் போகிறது. ஆறு புறவேற்றுமை வடிவங்களிலும் நான்கு ஆக்சிசனேற்ற நிலைகளிலும் புளுட்டோனியம் காணப்படுகிறது. கார்பன், ஆலசன்கள், நைட்ரசன், சிலிக்கான் ஐதரசன் போன்ற தனிமங்களுடன் புளுட்டோனியம் வினைபுரிகிறது. காற்றில் உள்ள ஈரத்துடன் சேர்ந்து ஆக்சைடுகளாகவும் நீரேற்றுகளாகவும் உருவாகி 70% அளவிற்கு கன அளவில் விரிவடைகிறது. இத்தனிமம் கதிரியக்கத் தன்மை கொண்டிருப்பதாலும் அது எலும்புகளில் திரளும் என்பதாலும் கையாள்வதற்கு அபாயமானதாக கருதப்படுகிறது.
1940 ஆம் ஆண்டு டிசம்பர் 14 ஆம் தேதி கலிபோர்னியாவின் பெர்க்லி பல்கலைக்கழகத்தில் 60-அங்குல சைக்ளோட்ரானில் யூரேனியம்-238 ஐசோடோப்பை டியூட்டிரான் குண்டுவீச்சினால் தாக்கப்பட்டபோது புளுட்டோனியம் முதலில் உற்பத்தி செய்யப்பட்டது. அரை வாழ்வுக் காலம் 2.1 நாட்கள் மட்டுமே கொண்ட முதலாவது நெப்டியூனியம்- 238 ஐசோடோப்பு தயாரிக்கப்பட்டபோது அது பின்னர் பீட்டா சிதைவுக்கு உட்பட்டு அணு எண் 94 உம் அணு எடை 238 உம் அரைவாழ்வுக் காலம் 87.7 ஆண்டுகளும் கொண்ட இப்புதிய தனிமம் உருவானது. யுரேனசு கோளை அடிப்படையாகக் கொண்டு யுரேனியத்தின் பெயரும், நெப்டியூன் கோளை அடிப்படையாகக் கொண்டு நெப்டியூனியமும், புளுட்டோ கோளை அடிப்படையாகக் கொண்டு புளுட்டோனியமும் பெயர்களாக வைக்கப்பட்டன. போர்க்கால நடவடிக்கைகள் காரணமாக 1948 ஆம் ஆண்டு வரை இத்தனிமத்தின் கண்டுபிடிப்பு அறிவிக்கப்படாமல் பாதுகாக்கப்பட்டது. புளுட்டோனியம் என்ற தனிமம் இயற்கையில் தோன்றும் தனிமங்களில் அதிக அணு எண் கொண்ட தனிமமாக கருதப்படுகிறது. U-238 படிவுகளில் சுவடு அளவுக்கு புளுட்டோனியம் காணப்படுகிறது. 1945 ஆம் ஆண்டு முதல் பூமியில் மிகவும் பொதுவாக புளுட்டோனியம் நியூட்ரான் பிடிப்பு மற்றும் பீட்டா சிதைவு போன்ற செயல்பாடுகளால் தோன்றி காணப்படுகிறது.
புளுட்டோனியம்-239 மற்றும் புளுட்டோனியம் -241 ஆகிய இரண்டு ஐசோடோப்புகளும் பிளவுறும் தன்மையைப் பெற்றுள்ளன. இதன் பொருள் அணுக்கரு தொடர் வினைகளை இவை தக்க வைத்துக் கொள்கின்றன என்பதாகும்.அணு ஆயுதங்கள் மற்றும் அணு உலைகளில் இவ்ற்றின் பிளவுறும் தத்துவம் பயன்படுகின்றன. புளுட்டோனியம் -240 எந்தவொரு மாதிரியின் பகுதிப்பொருளாக இருந்தாலும் அது அதிகவீதத்தில் நியூட்ரான் கற்றையை உமிழ்ந்து தன்னிச்சையாகப் பிளவுறுகிறது. ஒரு புளுட்டோனிய மாதிரியில் புளுட்டோனியம் -240 இருப்பது அதை ஓர் ஆயுதத்தில் பயன்படுத்துவதை கட்டுப்படுகிறது. அல்லது உலை எரிபொருளாக இருக்கக்கூடிய அதன் தரத்தையும் கட்டுப்படுத்துகிறது, மற்றும் புளூடானியம்- 240 இன் இருப்பு சதவிகிதம் அந்த ஆயுதத்தின் தரத்தையும் ஆயுட்காலத்தையும் நிர்ணயிக்கிறது. புளுட்டோனியம்-238 ஐசோடோப்பின் அரைவாழ்வுக் காலம் 88 ஆண்டுகளாகும். இது ஆல்பா துகள்களை உமிழ்கிறது. கதிரியக்க ஐசோடோப்பு வெப்பமின் மின்னாக்கிகளில் இது வெப்ப மூலமாக பயன்படுகிறது. இம்மின்னாக்கிகள் சிலவகை விண்கலன்களில் மின்னாற்றலை வழங்குகின்றன. புளுட்டோனியம் ஐசோடோப்புகள் விலை உயர்ந்தவையாகும். மேலும் அவற்றைப் பிரித்துப் பயன்படுத்துவதும் சிக்கலான செயல்முறையாகும். எனவே குறிப்பிட்ட ஒரு புளுட்டோனியம் ஐசோடோப்பு சிறப்பாக வ்டிவமைக்கப்பட்ட உலைகளில் தயாரித்துக் கொள்ளப்படுகின்றன.
பயனுள்ள அளவுகளில் புளுட்டோனியம் தயாரிப்பது முதல் முறையாக இரண்டாம் உலகப்போரின் போது மன்காட்டன் திட்டத்தின் ஒரு முக்கிய பகுதியாக இருந்தது, அப்போது முதல் அணு குண்டுகள் உருவாக்கப்பட்டன. சூலை1945 இல் நிகழ்த்தப்பட்ட டிரினிட்டி அணுகுண்டு சோதனையில் குண்டு மனிதன் வகை அணுகுண்டுகள் பயன்படுத்தப்பட்டன. மற்றும் ஆகத்து 1945 இல் நாகசாகியில் அணுகுண்டு வீச்சும் நிகழ்த்தப்பட்டது இவ்விரண்டு குண்டுகளிலும் புளுட்டோனியம் கருக்கள் இருந்தன. புளுட்டோனியத்தை ஆய்வுசெய்யும் மனிதர் மீதான கதிர்வீச்சு சோதனைகள் அவர்களுக்கு அறிவுறுத்தப்படாத முறையில் நடத்தப்பட்டன, போருக்குப் பின் பல மோசமான விபத்துக்கள், சில உயிரிழப்புகள் ஏற்பட்டன. அணுக்கரு உலைகளில் இருந்து புளுட்டோனியம் கழிவுப்பொருட்களை அகற்றுதல், பனிப்போரின் போது கட்டப்பட்ட அணுவாயுதங்களை அகற்றுவது போன்றவை அணுசக்தி பெருக்கத்தால் சுற்றுச்சூழலை பாதிக்கும் தன்மையை கொண்டடுள்ளன. மற்ற புளுட்டோனியம் ஆதாரங்கள் தற்போது தடை செய்யப்பட்டுள்ளன.
பண்புகள்
இயற்பியல் பண்புகள்
புளுட்டோனியம் பெரும்பாலான உலோகங்களைப் போல வெள்ளிய வெண்மை நிறங்கொண்டு நிக்கலைப் போல் பிரகாசமாக தோன்றுகிறது. ஆனால் இது காற்றில் ஆக்சிசனேற்றம் அடைந்து விரைவில் மங்கி சாம்பல் நிறம் அல்லது ஆலிவ் பச்சை அல்லது மஞ்சள் நிறத்திற்கு மாறுகிறது [1][2]. அறைவெப்ப நிலையில் புளுட்டோனியம் அதனுடைய ஆல்பா வடிவத்தில் உள்ளது. இதுவே புளுட்டோனியத்தின் மிகப்பொதுவான கட்டமைப்பு வடிவமாகும். இவ்வடிவ புளுட்டோனியம் கடினத்தன்மையும் நொருங்கும் தன்மையும் கொண்டதாக உள்ளது. வெப்பம் அல்லது மின்சாரத்தை இது நன்கு கடத்தாது. குறைவான உருகுநிலையாக 640 பாகை செல்சியசு வெப்பநிலையையும் உயர் கொதிநிலையாக 3228 பாகை செல்சியசு வெப்பநிலையையும் புளுட்டோனியம் பெற்றுள்ளது [1].
புறவேற்றுமை வடிவங்கள்
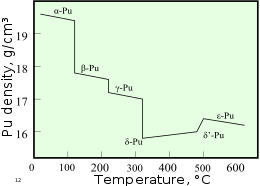
புளுட்டோனியம் சுற்றுப்புறஅழுத்தம் மற்றும் வெப்பநிலையில்கூட பல்வேறு வகையான புறவேற்றுமை வடிவங்களில் காணப்படுகிறது. பரவலாக இவை படிகக்கட்டமைப்பு மற்றும் அடர்த்தியில் வேறுபடுகின்றன. α மற்றும் δ புறவேற்றுமைகளுக்கிடையில் 25 சதவீதத்திற்கும் அதிகமான வேறுபாடுகள் காணப்படுகின்றன. புளுட்டோனியம் பொதுவாக ஆறு புறவேற்றுமை வடிவங்களைக் கொண்டுள்ளது. ஒரு குறிப்பிட்ட அழுத்த வரம்பிற்குள் ஓர் உயர் வெப்பநிலையில் ஏழாவது (சீட்டா, ζ) புறவேற்றுமை வடிவத்தை உருவாக்குகிறது. இந்த புறவேற்றுமை வடிவங்கள் அனைத்தும் வெவ்வேறு கட்டமைப்பு மாற்றங்கள் அல்லது ஒரு தனிமத்தின் வெவ்வேறு வகைகளாக மிகவும் ஒத்த உள் ஆற்றல்களைக் கொண்டிருக்கின்றன. ஆனால் கணிசமாக மாறுபடும் அடர்த்தி மற்றும் படிக கட்டமைப்புகளைக் கொண்டுள்ளன. இவை வெப்பநிலை, அழுத்தம் அல்லது வேதியியலில் ஏற்படும் மாற்றங்களுக்கு புளுட்டோனியத்தை மிகவும் உணர்திறன் மிக்க தனிமமாக்குகின்றன. மேலும் ஒரு புறவேற்றுமை வடிவத்திலிருந்து மற்றொரு வடிவத்திற்கு நிலை மாற்ற வியத்தகு அளவு மாற்றங்களை புளுட்டோனியம் அனுமதிக்கிறது. வெவ்வேறு புறவேற்றுமை வடிவங்களின் அடர்த்தி 16.00 கிராம் / செ.மீ 3 முதல் 19.86 கிராம் / செ 3 வரை மாறுபடுகிறது.
இந்த பல புறவேற்றுமை வடிவங்களின் இருப்பு புளுட்டோனியத்தை எந்திரமயமாக்குவது மிகவும் கடினமாகிறது. ஏனெனில் இது புறவேற்றுமை நிலையை மிக எளிதாக மாற்றுகிறது. எடுத்துக்காட்டாக, அறை வெப்பநிலையில் பயன்படுத்தப்படாத புளுட்டோனியம் α வடிவத்தில் உள்ளது. இது வார்ப்பிரும்பை ஒத்த எந்திர பண்புகளைக் கொண்டுள்ளது. ஆனால் சற்றே உயர் வெப்பநிலையில் நெகிழி மற்றும் இணக்கமான β (பீட்டா) வடிவத்திற்கு மாறுகிறது. சிக்கலான கட்ட வரைபடத்திற்கான காரணங்கள் முழுமையாக புரிந்து கொள்ளப்படவில்லை. ஆல்பா வடிவம் குறைந்த-சமச்சீர் ஒற்றைச்சாய்வு கட்டமைப்பைக் கொண்டுள்ளது, எனவே அது உடையக்கூடிய தன்மை, வலிமை, அமுக்கக்கூடிய தன்மை மற்றும் மோசமான வெப்ப கடத்துத்திறன் ஆகியனவற்றை வெளிப்படுத்துகிறது. δ (டெல்டா) வடிவத்தில் உள்ள புளுட்டோனியம் பொதுவாக 310 ° செல்சியசு முதல் 452 ° செல்சியசு வரையிலான வெப்ப வரம்பில் காணப்படுகிறது. ஆனால் ஒரு சிறிய சதவீத காலியம், அலுமினியம் அல்லது சீரியத்துடன் கலக்கும்போது அறை வெப்பநிலையில் அது நிலைப்புத்தன்மையைப் பெறுகிறது. அதன் வேலைத்திறன் மேம்படுகிறது மற்றும் பற்றவைப்பில் பயன்படுகிறது. δ வடிவ புளுட்டோனியம் குறிப்பாக உலோகத்தன்மை மிக்கதாக இருப்பினும் அலுமினியம் அளவுக்கு வலைமையான கம்பியாக இதை இழுக்கலாம். அணுக்கரு பிளவு வகை ஆயுதங்களில், புளூட்டோனியம் உள்ளகத்தை அமுக்கப் பயன்படும் வெடிக்கும் அதிர்ச்சி அலைகள் வழக்கமான δ கட்ட புளுட்டோனியத்தை அடர்த்தியான α வடிவத்திற்கு மாறுவதற்கு வழிவகுக்கிறது. மிக உயர்ந்த வெப்பநிலை திண்ம புறவேற்றுமை வடிவ புளுட்டோனியத்தை மற்ற தனிமங்களுடன் ஒப்பிடும்போது இது ஒழுங்கற்ற உயர் அணு சுய விரவலை வெளிப்படுத்துகிறது.
காலியம், அலுமினியம், அமெரிசியம், இசுக்காண்டியம் மற்றும் சீரியம் போன்ற தனிமங்கள் அறை வெப்பநிலையில் புளுட்டோனியத்தின் δ நிலையை நிலைப்புத்தன்மை உடையதாக மாற்ற முடியும். சிலிக்கான், இண்டியம், துத்தநாகம் மற்றும் சிர்கோனியம் ஆகியவை விரைவாக குளிர்விக்கும்போது சிற்றுறுதி நிலை δ நிலை புளுட்டோனியம் உருவாக அனுமதிக்கின்றன. அதிக அளவு ஆபினியம், ஒல்மியம்ம் மற்றும் தாலியம் ஆகியவை அறை வெப்பநிலையில் சிறிதளவு δ நிலையை தக்கவைக்க அனுமதிக்கின்றன. அதிக வெப்பநிலையில் α நிலை புளுட்டோனியத்தை நிலைத்திருக்க வைக்கும் ஒரே தனிமம் நெப்டியூனியம் மட்டுமேயாகும். தைட்டானியம், ஆபினியம் மற்றும் சிர்க்கோனியம் போன்ற தனிமங்கள் விரைவாக குளிர்ச்சியடையும் போது அறை வெப்பநிலையில் β கட்டத்தை உறுதிப்படுத்துகின்றன [3].
மேற்கோள்கள்
- "Plutonium, Radioactive". Wireless Information System for Emergency Responders (WISER). Bethesda (MD): U.S. National Library of Medicine, National Institutes of Health. பார்த்த நாள் November 23, 2008. (public domain text)
- "Nitric acid processing". Actinide Research Quarterly (Los Alamos (NM): Los Alamos National Laboratory) (3rd quarter). 2008. http://www.lanl.gov/discover/publications/actinide-research-quarterly/. பார்த்த நாள்: February 9, 2010. "While plutonium dioxide is normally olive green, samples can be various colors. It is generally believed that the color is a function of chemical purity, stoichiometry, particle size, and method of preparation, although the color resulting from a given preparation method is not always reproducible.".
- Hecker, Siegfried S. (2000). "Plutonium and its alloys: from atoms to microstructure" (PDF). Los Alamos Science 26: 290–335. https://fas.org/sgp/othergov/doe/lanl/pubs/00818035.pdf.
புற இணைப்புகள்
- "Alsos Digital Library for Nuclear Issues - Plutonium". Washington and Lee University.
- Sutcliffe, W. G. (1995). "A Perspective on the Dangers of Plutonium". Lawrence Livermore National Laboratory. மூல முகவரியிலிருந்து September 29, 2006 அன்று பரணிடப்பட்டது.
- Johnson, C. M. (1997). "Nuclear Weapons: Disposal Options for Surplus Weapons-Usable Plutonium". CRS Report for Congress # 97-564 ENR. பார்த்த நாள் February 15, 2009.
- "Physical, Nuclear, and Chemical, Properties of Plutonium". IEER (2005). பார்த்த நாள் February 15, 2009.
- Bhadeshia, H.. "Plutonium crystallography".
- Samuels, D. (2005). "End of the Plutonium Age". Discover Magazine 26 (11). http://discovermagazine.com/2005/nov/end-of-plutonium.
- Pike, J. (2000). "Plutonium production". Federation of American Scientists. மூல முகவரியிலிருந்து February 3, 2009 அன்று பரணிடப்பட்டது. பார்த்த நாள் February 15, 2009.
- "Plutonium Manufacture and Fabrication". Nuclearweaponarchive.org.
- Ong, C. (1999). "World Plutonium Inventories". Nuclear Files.org. மூல முகவரியிலிருந்து August 5, 2014 அன்று பரணிடப்பட்டது. பார்த்த நாள் February 15, 2009.
- "Challenges in Plutonium Science". Los Alamos Science I & II (26). 2000. https://fas.org/sgp/othergov/doe/lanl/pubs/number26.htm. பார்த்த நாள்: February 15, 2009.
- "Plutonium". Royal Society of Chemistry. பார்த்த நாள் February 6, 2015.
- "Plutonium". University of Nottingham. பார்த்த நாள் February 6, 2015.
வார்ப்புரு:Subject bar