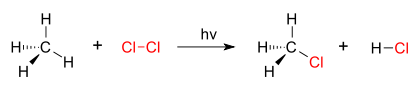பதிலீட்டு வினை
பதிலீட்டு வினை (Substitution reaction) என்பது ஒரு வேதிச் சேர்மத்தில் உள்ள வேதி வினைக்குழுவானது மற்றொரு வேதி வினைக்குழுவால் இடப்பெயர்ச்சி செய்யப்படும் ஒரு வேதி வினையாகும்.[1][2] பதிலீட்டு வினைகளானவை கரிம வேதியியலில் மிகுந்த முக்கியத்துவம் வாய்ந்தவையாகும். கரிம வேதியியலில் பதிலீட்டு வினைகள் எலக்ட்ரான் கவர் வினை அல்லது கருக்கவர் வினை என வினையில் ஈடுபடும் வேதிக்காரணிகளைப் பொறுத்து இரண்டு வகைப்படும். இவை தவிர கீழே குறிப்பிடப்பட்டுள்ளவாறு இன்னும் சில வகைப்பாடுகளும் உள்ளன.
கரிம பதிலீட்டு வினைகளானவை பல முக்கிய கரிம வினை வகைகளின் படியாக வினையில் ஈபடுகின்ற வினைப்பொருட்கள் எலக்ட்ரான் கவர் பொருளா அல்லது கருக்கவர் பொருளால் பதிலீட்டு வினையை நிகழ்த்துகிறதா? வினை இடைப்பொருளானது கார்பன் நேரயனியா? அல்லது கார்பன் எதிரயனியா? அல்லது தனி உறுப்பா? அல்லது வினைவேதிமம் அலிபாட்டிக் வகையைச் சார்ந்ததா? அரோமேடிக் வகையைச் சார்ந்ததா? என்பதைப் பொறுத்து வகைப்படுத்தப்படுகின்றன. விரிவான அளவில் வினை வகையைப் புரிந்து கொள்வது, வினையின் விளைவாக கிடைக்கப் போகின்ற விளைபொருளைத் தீர்மானிக்க உதவுகிறது. வினையின் வகையை அடையாளம் காண்பது வினை நிகழத் தேவையான மாறிகளான வெப்பநிலை மற்றும் தகுந்த கரைப்பானைத் தேர்ந்தெடுத்தல் போன்றவற்றிற்கு உதவுகிறது.
பதிலீட்டு எதிர்வினையின் ஒரு நல்ல உதாரணம் ஆலசனேற்றம் ஆகும். குளோரின் வாயு (Cl-Cl) கிளர்வுறச் செய்யப்பட்டால், சில மூலக்கூறுகள் இரண்டு குளோரின் தனி உறுப்புகளாக (Cl.) பிளவுறுகின்றன. இந்த கட்டற்ற எலக்ட்ரான்கள் வலுவான கருக்கவர் தன்மை கொண்டவை ஆகும். இத்தகைய தனி உறுப்புகள் பலவீனமான C-H சகப்பிணைப்பை உடைத்து, விடுவிக்கப்பட்ட புரோட்டானை மின்சுமையற்ற நடுநிலை H-Cl மூலக்கூறுகளை உருவாக்குகிறது. மற்ற தனி உறுப்புகள் CH3 தொகுதியுடன் மீண்டும் சகப்பிணைப்பை உருவாக்கி மெதில் குளோரைடை உருவாக்குகின்றன.
|
|
| மீத்தேனின் குளோரினேற்றம் |
|---|
கருக்கவர் பதிலீட்டு வினை
கரிம மற்றும் கனிம வேதியியலில், கருக்கவர் பதிலீட்டு வினை என்பது ஒரு அடிப்படை வகை வினையாகும். கருக்கவர் காரணியானது நேர்மின் சுமையுடைய அல்லது பகுதி நேர்மின் சுமையுடைய ஒரு அணு அல்லது அணுக்களின் தொகுதியைத தாக்குகின்ற அல்லது தேர்ந்தெடுத்து பிணைப்பை ஏற்படுத்திக் கொள்ளக்கூடிய ஒரு அடிப்படை வினையாகும். இவ்வாறு நிகழ்வதால், இது ஒரு பலவீனமான கருக்கவர் காரணியை இடப்பெயர்ச்சி செய்து விடுபட்டுச் செல்லும் தொகுதியாக மாறுகிறது. பின்னர் மீதமிருக்கிற நேர் அயனி அல்லது பகுதியளவு நேரயனியானது ஒரு எலக்ட்ரான் கவர் பொருளாக மாறுகிறது. எலக்ட்ரான் கருக்கவர் பொருள் மற்றும் விடுபடு தொகுதி இவை எந்த முழு மூலக்கூறுத் தொகுதியின் பகுதியாக உள்ளதோ அது வினைவேதிமம் எனப்படுகிறது.[1][2]
மிகவும் பொதுவான வினையின் வடிவமானது பின்வருமாறு தரப்படுகிறது. R-LG வினைவேதிமத்தைக் குறிக்கிறது.
- Nuc: + R-LG → R-Nuc + LG:
கருக்கவர் காரணியிலிருந்து(Nuc:) வரும் எதிர்மின்னி இரட்டையானது (:) வினைவேதிமத்தைத் (R-LG) தாக்கி ஒரு புதிய சகப்பிணைப்பை Nuc-R-LG உருவாக்குகிறது. விடுபடு தொகுதியானது ஒரு எதிர்மின்னி இரட்டையுடன் விடுபட்டுச் செல்லும் போது முந்தைய நிலையின் மின்சுமையானது தக்க வைக்கப்படுகிறது. இதில் முதன்மையான விளைபொருளாக R-Nuc உள்ளது. இத்தகைய வினைகளில், கருக்கவர் காரணியானது, வழக்கமாக, மின்சுமைகளின் அடிப்படையில் நடுநிலைத்தன்மை உடையதாகவோ அல்லது எதிர்மின் சுமை உடையதாகவோ இருக்கிறது. வினைவேதிமமானது மின்சுமையினடிப்படையில் நடுநிலைத்தன்மை உடையதாகவோ அல்லது நேர்மின் சுமை உடையதாகவோ இருக்கிறது.
கருக்கவர் பதிலீட்டு வினையின் உதாரணமானது, காரத்தின் முன்னிலையில் அல்கைல் புரோமைடின் (R-Br) நீராற்பகுப்பு வினையாகும். இந்த வினையில் கார OH− தொகுதியானது தாக்குகின்ற கருக்கவர் காரணியாகவும் மற்றும் விடுபடு தொகுதியானது Br− ஆகவும் உள்ளது.
- R-Br + OH− → R-OH + Br−
கரிம வேதியியலில், கருக்கவர் பதிலீட்டு வினைகள் பொதுவான இடத்தை வகிக்கின்றன. மேலும் அவை நிறைவுற்ற அலிபாட்டிக் சேர்மங்களில் நடப்பவை அல்லது மிகச்சில நேரங்களில் அரோமேடிக் அல்லது இதர நிறைவுறாத கார்பன் மையங்களில் நிகழ்பவை எனப் பொதுவாக வகைப்படுத்தப்படுகின்றன.
மேற்கோள்கள்
- March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3rd ), New York: Wiley, பன்னாட்டுத் தரப்புத்தக எண்:0-471-85472-7
- Imyanitov, Naum S. (1993). "Is This Reaction a Substitution, Oxidation-Reduction, or Transfer?". J. Chem. Educ. 70 (1): 14–16. doi:10.1021/ed070p14. Bibcode: 1993JChEd..70...14I.